
- •Дисклеймер
- •Информация о раскрытии финансовой заинтересованности
- •Противовирусные препараты прямого действия (ПППД)
- •Увеличение частоты цирроза печени в исходе ХГС в России к 2030 году
- •Наличие цирроза печени у больного ХГС - наивысший приоритет назначения противовирусной терапии, учитывая
- •Наличие цирроза печени, особенно с декомпенсацией функции печени, резко сокращает продолжительность жизни пациентов
- •Большинство больных ХГС с наличием цирроза печени – люди трудоспособного возраста
- •По результатам оценки бремени ХГС в РФ в 2010 г – его наибольшая
- •Достижение УВО снижает риск смерти больных ХГС с циррозом печени на 74%
- •Grazoprevir/Elbasvir
- •Исследования 2b-3 фазы
- •Популяции пациентов с ХГС с компенсированным циррозом, участвовавшие в исследованиях GZR/EBR
- •Эффективность EBR/GZR при компенсированном циррозе печени не уступает эффективности при отсутствии цирроза
- •Эффективность терапии EBR/GZR у пациентов
- •Эффективность терапии EBR/GZR пациентов с компенсированным
- •Эффективность EBR/GZR у пациентов с ВГС генотипа 1b1
- •Анализ безопасности терапии EBR/GZR пациентов с циррозом печени в исследованиях 2/3 фазы1
- •ПАЦИЕНТЫ С ГЕНОТИПОМ ВИРУСА 3:
- •C-ISLE: Пациенты с ХГС генотипа 3 и компенсированным циррозом печени
- •Нежелательные явления
- •ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ЭЛБАСВИРА/ГРАЗОПРЕВИРА У ПЕРВИЧНЫХ ПАЦИЕНТОВ С ХГС ГЕНОТИПОВ 1, 4 И
- •Сопоставимая эффективность GZR/EBR без РБВ
- •Частота УВО12 при генотипе 1b была высокой во всех странах, включая 99% эффективность
- •Эффективность EBR/GZR в реальной клинической
- •Эффективность и безопасность12 недель Элбасвира/Гразопревира
- •Актуальность проблемы
- ••Цель исследования: сравнение эффективности и безопасности 12 недель элбасвира/гразопревира у пациентов в возрасте
- •В анализ вошли данные 12 клинических исследований EBR/GZR
- •Исходные характеристики пациентов
- •Исходные характеристики пациентов
- •Исходные характеристики пациентов
- •Общие характеристики пациентов
- •Эффективность 12 недель терапии EBR/GZR
- •Изменение показателей скорости клубочковой
- •Выводы
- •Заключение

Достижение УВО снижает риск смерти больных ХГС с циррозом печени на 74%
- 74%
- 50% |
- 79% |
5-летняя смертность (95% доверительный интервал) для группы, достигшей УВО vs. группы, не достигшей устойчивого вирусологического ответа (УВО), для каждой когорты
RU-ZEP-00021 05.2019
Simmons B. et al. Clinical Infectious Diseases. 2015; 61(5): 730-40

Grazoprevir/Elbasvir
|
• |
Ингибитор NS3/4A |
• |
Ингибитор NS5A |
|
|
• |
100 мг один раз в день |
• |
50 мг, один раз в день |
|
|
|
|
|
|
|
Grazoprevir Elbasvir
(MK-5172) (MK-8742)
Комбинированный препарат с фиксированной дозой
Широкая активность против большинства генотипов ВГС in vitro1-3
Эффективен для первичных больных и для пациентов с неудачей предыдущей терапии, с циррозом и без цирроза с моноинфекцией ВГС и ко-инфекцией ВИЧ/ВГС 4,5
1.Summa V, et al. Antimicrobial Agent Chemother 2012:56;4161-67; 2. Coburn CA,, et al. ChemMedChem 2013; 8: 1930–40;
3. Harper S, et al. ACS Med Chem Lett. 2012 Mar 2;3(4):332-6RU.; 4-.ZEPLawitz-00021et al05. Lancet.2019 2015; 385:1075; 5. Sulkowski et al. Lancet 2015; 385:1087

Исследования 2b-3 фазы
Исследование |
Генотип |
N |
Цирроз |
ПВТ в |
|
Фоновое |
Схема |
|
анамнезе |
состояние |
(недели) |
|
|||||
C-EDGE TN |
1, 4, 6 |
421 |
± Цирроз |
Нет |
|
|
12, без РБВ |
|
|
|
|
|
|
|
|
|
|
C-EDGE CO-INFXN |
1, 4, 6 |
218 |
± Цирроз |
Нет |
|
ВИЧ |
12, без РБВ |
|
|
|
|
|
|
|
|
|
|
C-WORTHY G1 |
1b |
61 |
Без цирроза |
Нет |
|
|
8 ± РБВ |
|
|
|
|
|
|
|
|
|
|
C-SWIFT |
1, 3 |
42 |
± Цирроз |
Нет |
|
|
12 + Софосбувир |
|
|
|
|
|
|
|
|
|
|
C-EDGE TE |
1, 4, 6 |
420 |
± Цирроз |
«Двойная» |
±ВИЧ |
12 или 16, ±РБВ |
|
|
|
|
|
|
|
|
|
|
|
C-Salvage |
1 |
79 |
± Цирроз |
«Тройная» |
|
12, + РБВ |
|
|
|
|
|
|
|
|
|
|
|
C-SURFER |
1 |
237 |
± Цирроз |
Нет или |
ХБП 4-5 стадии |
12, без РБВ |
|
|
«двойная» |
|
|||||||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
C-EDGE CO-STAR |
1, 4, 6 |
301 |
± Цирроз |
Нет |
|
ЗТО, ±ВИЧ |
12, без РБВ |
|
|
|
|
|
|
|
|
|
|
C-EDGE H2H |
1 |
255 |
± Цирроз |
Нет или |
±ВИЧ |
12, без РБВ |
|
|
«двойная» |
|
|||||||
|
|
|
|
|
|
|
||
C-EDGE IBLD |
|
|
|
Нет или |
Наследственные |
|
|
|
1, 4, 6 |
161 |
± Цирроз |
заболевания |
12, без РБВ |
|
|||
«двойная» |
|
|||||||
|
|
|
|
крови |
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
«Двойная» - неудача терапии пегилированным |
ХБП 4-5: Хроническая |
ВИЧ – вирус |
РБВ - рибавирин |
|||||
интерфероном и рибавирином |
|
болезнь почек 4-5 стадии |
иммунодефицита |
|
|
|||
«Тройная» - неудача терапии пегилированным |
(включая пациентов на |
человека |
|
|
||||
интерфероном, рибавирином и ингибитором |
гемодиализе) |
|
ЗТО – заместительная |
|
|
|||
протеазы I поколения |
|
|
|
|
терапия опиатами |
|
|
|
RU-ZEP-00021 05.2019

Популяции пациентов с ХГС с компенсированным циррозом, участвовавшие в исследованиях GZR/EBR
Без опыта |
C неудачей |
|
«двойной» |
||
терапии1 |
||
терапии3 |
Пациенты с ВИЧ/ВГС7
Пациенты с генотипами
1, 4, 61,2,3,7
8 клинических исследований
~2000 пац.
>20 стран
C неудачей «тройной» терапии5
C болезнью почек 4/5 стадии4
Пациенты с |
С наследств |
генотипом |
болезнями |
36 |
крови2 |
1. Zeuzem et al. Ann Intern Med. 2015;163:1-13;. 2. Hezode C., et al.. J. Hepatol., 2016, .Suppl., A. SAT-128, P. 769 3. Kwo P et al. EASL 2015 #P0886. 4. Roth D. et al. Lancet. 2015 Oct 17;386(10003):1537-45. 5. Buti M. et al. ClinRU.-InfectZEP-.00021Dis., 2016,05.201962( ), 32-36. 6. Foster G. AASLD 2016 Nov 11-15
Boston, MA. 7. Rockstroh JK et al. Lancet HIV. 2015;2:e319-27
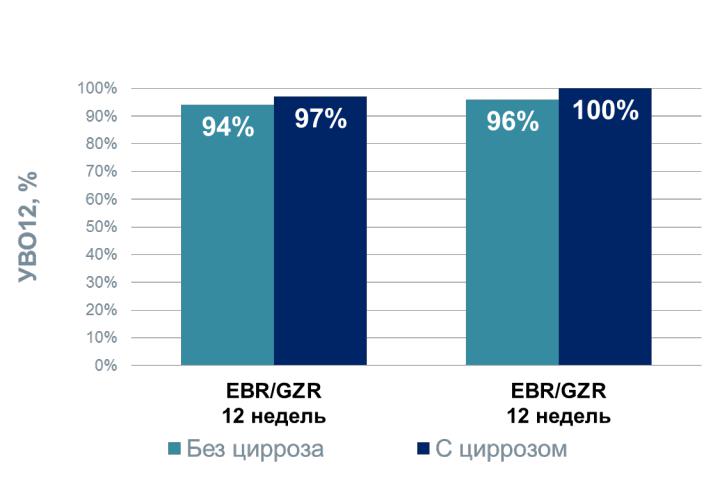
Эффективность EBR/GZR при компенсированном циррозе печени не уступает эффективности при отсутствии цирроза
Эффективность 12 недель терапии у пациентов с ХГС генотипа 1а, 1b и 4
C-EDGE TN1 |
C-EDGE CO-INFECTION2 |
n |
231 |
68 |
175 |
35 |
N |
246 |
70 |
183 |
35 |
RU-ZEP-00021 05.2019
1. Zeuzem et al. Ann Intern Med. 2015;163:1-13; 2 Rockstroh JK et al. Lancet HIV. 2015;2:e319-27.
Эффективность терапии EBR/GZR у пациентов
без опыта терапии с компенсированным циррозом печени
12 недель EBR/GZR для генотипа 1, 4
(Исследования C-EDGE Treatment Naïve, C-EDGE Coinfection)
% |
100 |
|
|
|
УВО12, |
|
|
|
|
|
|
|
||
75 |
|
|
|
|
|
50 |
|
|
|
|
25 |
|
|
|
135 |
|
73 |
||
|
|
|||
138 |
0 |
|
76 |
|
|
|
|
|
|
RU-ZEP-00021 05.2019
Ранняя отмена/потеря связи
УВО12(mFAS*)
Прорыв
Рецидив
96 |
100 |
100 |
73 |
|
56 |
6 |
|
76 |
6 |
56 |
6 |
|
|
|
|
|
|
|
6 |
|
|
|
Генотип 1a |
|
Генотип 1b |
|
Генотип 4 |
1* |
|
0 |
0 |
|
97% |
|
100% |
100% |
|
(73/75) |
|
(56/56) |
(6/6) |
|
1 |
|
0 |
0 |
|
1 |
|
0 |
|
0 |
|
|
|||
|
|
|
|
|
49
49
Jacobson I et al. AASLD 2015 #42. Poordad F et al. ILC 2015, oral presentation
*mFAS (modified full analysis set): исключены пациенты, прекратившие лечение по причинам не связанным с исследуемой терапией.

Эффективность терапии EBR/GZR пациентов с компенсированным |
|
пациентов |
циррозом печени и неудачей предыдущей терапии |
|
|
УВО12, %
100% |
|
|
|
|
|
|
94% |
97% |
|
94% |
98% |
||
90% |
|
|||||
80% |
|
|
|
|||
|
|
|
|
|
||
|
|
|
|
|
||
70% |
|
|
|
|
|
|
|
|
|
|
|
||
60% |
|
|
|
|
|
|
|
|
|
|
|
||
50% |
|
|
|
|
|
|
|
|
|
|
|
||
40% |
|
|
|
|
|
|
|
|
|
|
|
||
30% |
|
|
|
|
|
|
135 |
255 |
|
32 |
45 |
||
20% |
|
|||||
10% |
144 |
264 |
36 |
34 |
44 |
|
0% |
|
|
|
|
||
C-EDGE Ttreatment Experienced |
36 |
C-EDGE SALVAGE |
||||
|
||||||
|
|
|||||
|
|
Цирроз |
Без цирроза |
|
||
FAS (full analysis set): включены пациенты, получившие хотя бы 1 дозу исследуемого препарата
C-EDGE TE: неудача предыдущей двойной терапии; EBR/GZR 12/16 недель с и без РБВ EDGE SALVAGE: неудача предыдущей тройной терапии; EBR/GZR 12 недель с РБВ
1. |
C-EDGE TE: Kwo P et al. Gastroenterology 2017;152:164–175 |
RU-ZEP-00021 05.2019 |
|
2. |
C-EDGE SALVAGE: Forns X et al. J Hepatol. 2015;63:564-572 |
||
|
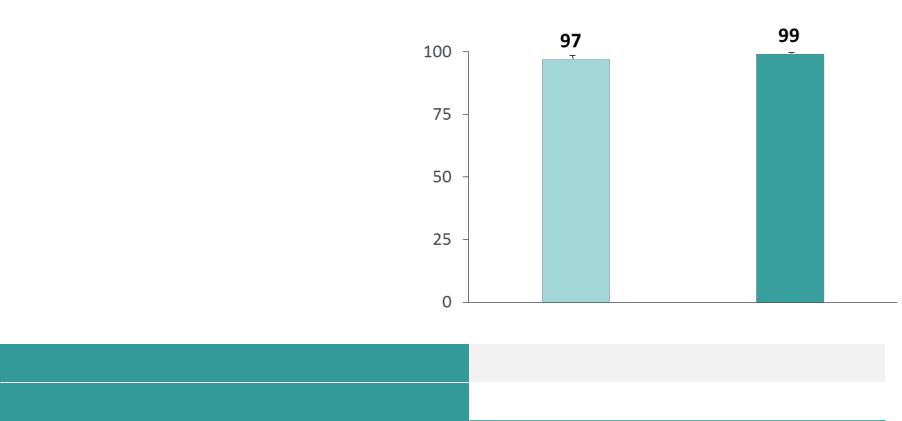
Эффективность EBR/GZR у пациентов с ВГС генотипа 1b1
•Данные интегрального вторичного анализа
•Включены результаты 1,070 пациентов из 30 стран и 11 клинических исследований 2/3 фазы
•Популяция пациентов
–Ранее не леченные и после неудачи предыдущей терапии;
–С ко-инфекцией ВИЧ-1 и без неё;
–Без цирроза печени или с компенсированным циррозом;
–С ХБП 4-5 стадий, включая находящихся на гемодиализе, и без неё (C-SURFER).
Частота УВО12 после 12 недель терапии EBR/GZR без РБВ
у пациентов с ВГС генотипа 1b
% |
|
99.5% (188/189, FAS) |
|
|
|
УВО12, |
|
|
|
||
|
с компенсированным |
|
|
||
|
|
|
|
||
|
|
циррозом достигли |
|
|
|
|
|
УВО12 |
|
|
|
|
|
|
|
|
|
|
|
1,040 |
1,040 |
|
|
|
|
1,070 |
1,055 |
|
|
1040 |
FAS |
a |
1040 |
b |
|
|
mFAS |
|
|||
1070 |
|
|
1055 |
|
|
Вирусологическая неудача: рецидив |
15 |
15 |
Невирусологическая неудача |
15 |
0 |
aFAS: включены пациенты, получившие хотя бы 1 дозу исследуемого препарата. RU-ZEP-00021 05.2019
bmFAS: исключены 15 пациентов, прекративших лечение по причинам не связанным с исследуемой терапией.
1. Zeuzem S et al. J Gastroenterol (2018) 53:679–688.

Анализ безопасности терапии EBR/GZR пациентов с циррозом печени в исследованиях 2/3 фазы1
|
EBR/GZR, |
EBR/GZR + |
Плацебо, |
||||
|
N=264 |
RBV, N=193 |
N=22* |
||||
НЯ, связанные с терапией, n (%) |
111( 42,0%) |
141 (73,1%) |
9 (40,9%) |
||||
|
|
|
|
|
|
|
|
Серьёзные НЯ, n (%) |
8 |
(3,0%) |
6 |
(3,1%) |
0 |
(0%) |
|
|
|
|
|
|
|
|
|
Серьёзные НЯ, связанные с терапией, |
1 |
(0,4%) |
0 |
(0,0%) |
0 |
(0%) |
|
n (%) |
|||||||
|
|
|
|
|
|
||
Смертьa, n (%) |
1 |
(0,4%) |
1 |
(0,5%) |
0 |
(0%) |
|
Отмена терапии из-за НЯ, n (%)b |
2 |
(0,8%) |
4 |
(2,1%) |
1 (4,5%) |
||
Отмена терапии из-за лабораторных |
|
|
|
|
|
|
|
НЯ, n (%) |
|
|
|
|
|
|
|
АЛТс |
1 |
(0,4%) |
0 |
(0,0%) |
0 (0,0%) |
||
Общ билирубин |
0 |
(0,0%) |
1 |
(0,5%) |
0 (0,0%) |
||
|
|
|
|
|
|
|
|
Частые НЯ (>10%) |
|
|
|
|
|
|
|
Слабость |
40 |
(15,2%) |
59 |
(30,6%) |
18 |
(17%) |
|
|
|
|
|
|
|
|
|
Головная боль |
44 |
(16,7%) |
40 |
(20,7%) |
19 |
(18%) |
|
|
|
|
|
|
|||
Тошнота |
11 (4,2%) |
26 |
(13,5%) |
8 (7,6%) |
|||
|
|
|
|
|
|
|
|
a Смерть: ИБС, ДТП, лимфома, все не связаны с препаратом; bОтмена из-за непереносимости: EBR/GZR: лимфома, повышение АЛТ; EBR/GZR+RBV: маточное кровотечение, тахикардия, депрессия, тромбоз воротной вены/колит; сОтмена терапии из-за лабораторных НЯ: повышение АЛТ и эозинофилия. 
*Данные исследования C-EDGE Treatment Naïve: Zeuzem S. et al. Ann Intern Med. 2015;163:1-13.
Jacobson I et al. Gastroenterology 2017;152:1372–1382. RU-ZEP-00021 05.2019
ПАЦИЕНТЫ С ГЕНОТИПОМ ВИРУСА 3:
Исследование C-ISLE
Анализ эффективности терапии GZR/EBR + SOF у пациентов с ХГС генотипа 3
RU-ZEP-00021 05.2019

Эффективность терапии EBR/GZR + SOF у пациентов
с ХГС генотипа 3 и компенсированным циррозом печени
C-ISLE: дизайн и пациенты |
|
|
Схема терапии |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• EBR/GZR в 1 таблетке (50 мг/100 мг) |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
• SOF (400 мг) |
||||||||
100 пациентов с ХГС генотипа 3 и циррозом печени |
|
|
• РБВ (800-1400 мг/в день) |
|||||||||||||||||||||||||||||
Без опыта |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
EBR/GZR + SOF + |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
УВО12 |
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
терапии, |
РБВ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N=47 |
EBR/GZR + SOF |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
УВО12 |
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
После неудачи терапии пегИФН + РБВ, N=53
EBR/GZR + SOF |
УВО12 |
EBR/GZR + SOF + РБВ |
УВО12 |
EBR/GZR + SOF |
УВО12 |
0 |
4 неделя |
8 неделя |
12 неделя |
16 неделя |
12 недель после |
|
окончания терапии |
||||||
|
|
|
|
|
RU-ZEP-00021 05.2019
Foster G. et al. HEPATOLOGY, Vol. 67, No. 6, 2018
