
Постнагрузка
Это нагрузка сопротивлением току крови при изгнании её из полости желудочка. В клинической практике мерой постнагрузки является величина общего легочного сопротивления (ОЛС) для МКК, равная в норме 150-350 дин*с*см-5, и общего периферического сосудистого сопротивления (ОПСС) для БКК, равная в норме 1200-1700 дин*с*см-5. Косвенным признаком изменения постнагрузки для левого желудочка может быть величина АДср, равная в норме 80-95 мм Hg.
Однако в физиологии классическим представлением о постнагрузке является давление над полулунными клапанами перед изгнанием крови желудочками. Иными словами это конечно-диастолическое давление над полулунными клапанами в легочной артерии и аорте. Естественно, чем больше периферическое сопротивление сосудов, тем больше конечно-диастолическое давление над полулунными клапанами.
Увеличение постнагрузки.
Такая ситуация возникает при функциональном сужении артериальных периферических сосудов, хоть в МКК, хоть в БКК. Она может быть обусловлена органическими изменениями в сосудах (первичная лёгочная гипертензия или гипертоническая болезнь). Это может быть при сужении выходного отдела из правого или левого желудочка (подклапанные, клапанные стенозы).
Закон, по которому желудочек приспосабливается к нагрузке сопротивлением, впервые открыл Г.Анреп (1912г., лаборатория Е.Старлинга).
Дальнейшие исследования этого закона были продолжены самим Е.Старлингом и далее многими известными физиологами. Результаты каждого исследования были опорой и толчком к следующему.
Г. Анреп установил, что при увеличении сопротивления в аорте, вначале кратковременно объём сердца увеличивается (похоже на приспособительную реакцию О.Франка и Е.Старлинга). Однако затем объём сердца постепенно уменьшается до новой, больше исходной, величины и далее остается стабильным. При этом, несмотря на увеличение сопротивления в аорте, УО остается прежним.
Приспособительную реакцию сердца по закону Г. Анрепа и А. Хилла при увеличении нагрузки сопротивлением Ф.З.Меерсон объясняет следующим образом (1968 г.): по мере повышения нагрузки сопротивлением количество актиномиозиновых связей увеличивается. А количество свободных центров, способных реагировать между собой, в актиновых и миозиновых волокнах уменьшается. Поэтому с каждой, всё большей, нагрузкой количество вновь образующихся актиномиозиновых связей уменьшается в единицу времени.
Одновременно уменьшается и скорость сокращения, и количество механической и тепловой энергии, освобождающейся при распаде актиномиозиновых связей, постепенно приближаясь к нулю.
Очень важно, что количество актиномиозиновых связей увеличивается, а их распад уменьшается. Это означает, что с увеличением нагрузки наступает пересократимость актиномиозиновых волокон, что и ограничивает эффективность работы сердца.
Итак, когда нагрузка сопротивлением увеличивается на 40-50%, адекватно ей увеличивается мощность и сила мышечного сокращения. При большем увеличении нагрузки эффективность этой приспособительной реакции утрачивается из-за потери мышцей способности расслабляться.
Другим фактором, со временем ограничивающим эту приспособительную реакцию, является, как было установлено Ф.З.Меерсоном и его сотрудниками (1968 г.), снижение сопряжения окисления и фосфорилирования на 27-28% на участке – «цитохром с» - «кислород», при этом в миокарде уменьшается количество АТФ и особенно креатинфосфата (КФ).
Значит, закон Г. Анрепа и А. Хилла обеспечивает приспособление сердечной мышцы к нагрузке сопротивлением путём увеличения мощности желудочка, приводящей к увеличению силы сокращения без изменения исходной длины мышечного волокна.
Приспособительную реакцию Г. Анрепа и А. Хилла S.Sarnoff назвал гомеометрической регуляцией (homoios по греч. - подобный; применительно к теме раздела - регуляция посредством такой же длины волокна).
Здесь также важен вопрос: можно ли усилить эффект закона Г. Анрепа и А. Хилла? Исследования E.H. Sonnenblick (1962-1965 г.г.) показали, что при чрезмерной постнагрузке миокард способен увеличивать мощность, скорость и силу сокращения под воздействием положительно инотропных средств. Уменьшение постнагрузки.
Связано с уменьшением давления над полулунными клапанами. При нормальном ОЦК уменьшение постнагрузки становится возможным только при единственном обстоятельстве - при увеличении объема сосудистого русла, т.е. при сосудистой недостаточности.
Уменьшение давления над полулунными клапанами способствует укорочению периода повышения внутрижелудочкового давления и уменьшению самой величины этого давления перед началом изгнания крови. Это уменьшает потребность миокарда в кислороде и его энергозатраты на напряжение.
Однако все это уменьшает линейную и объемную скорость кровотока. В связи с этим уменьшается и венозный возврат, что ухудшает наполнение желудочков. В таких условиях единственно возможной приспособительной реакцией становится увеличение ЧСС, направленное на поддержание СВ. Как только тахикардия станет сопровождаться снижением СВ, эта приспособительная реакция переходит в разряд патологической.
Совокупность всех исследований, выполненных О.Франком, Е.Старлингом, Г.Анрепом, А.Хиллом и другими физиологами того периода позволила выделить два варианта сокращения сердечного волокна: изотоническое и изометрическое сокращения.
В соответствии с этим выделены два варианта работы желудочков сердца.
1. Когда желудочек работает преимущественно с нагрузкой по объему - он работает по варианту изотонического сокращения. При этом тонус мышцы изменяется в меньшей мере (изотония), преимущественно изменяется длина и поперечное сечение мышцы.
2. Когда желудочек работает преимущественно с нагрузкой по сопротивлению - он работает по варианту изометрического сокращения. При этом преимущественно изменяется напряжение мышцы (тонус), а её длина и поперечное сечение изменяются в меньшей мере или почти не изменяются (изометрия).
При работе желудочка с нагрузкой по сопротивлению (даже при функциональном изменении ОЛС или ОПСС) многократно увеличивается потребность миокарда в кислороде. Поэтому исключительно важным является обеспечение такого больного в первую очередь кислородом.
Врачам нередко приходится усиливать работу сердца инотропными средствами. В физиологии кровообращения (в т.ч. и клинической) под инотропизмом понимается (Ф.З. Меерсон, 1968 г.) регулирование скорости сокращения и расслабления, и поэтому мощности и эффективности работы сердца при неизменных размерах желудочка.
Инотропизм направлен не на сверхнормальное увеличение силы сокращений сердца, а на поддержание силы сокращений, в лучшем случае близкой к норме.
Инотропизм отличается от закона О.Франка и Е.Старлинга тем, что при этом не изменяется исходная длина волокон миокарда. Он отличается от закона Г. Анрепа и А. Хилла тем, что при этом увеличивается не только скорость сокращения, но и (главное!) скорость расслабления волокон миокарда (чем предупреждается пересократимость, или контрактура, миокарда).
Однако при искусственной инотропной регуляции работы сердца норадреналином и др. аналогичными средствами может быть серьезная опасность. Если резко и значительно уменьшить введение инотропного средства или прекратить введение его, то может резко снизиться тонус миокарда.
Возникает острая тоногенная дилатация желудочка. Его полость увеличивается, резко снижается внутрижелудочковое давление. В этих условиях, чтобы достигнуть прежней величины напряжения необходимы большие затраты энергии.
Процесс наращивания напряжения является самым главным потребителем энергии в сердечном цикле. Кроме того, он идет в первую очередь. В физиологии существует закон, что первый процесс всегда старается как можно полнее использовать наличную энергию, чтобы завершить его целиком и полностью. Остаток энергии расходуется на выполнение следующего процесса и т.д. (т.е. каждый предыдущий процесс как Людовик XV: "после нас хоть потоп").
За процессом увеличения напряжения идет работа по перемещению крови из желудочков в сосуды. Из-за того, что на напряжение затрачивается почти вся наличная энергия, а на изгнание ее недостает, от напряжения начинает отставать работа желудочков по перемещению крови. В результате общая эффективность сердца снижается. С каждым таким неполноценным сокращением прогрессивно увеличивается остаточный объем крови в полости желудочка и, в конце концов, наступает асистолия.
Каппиляры
Главный интерес к капиллярам связан с тем, что в них происходит обмен между кровью и интерстициальной жидкостью. У среднего человека имеется примерно 40 млд. капилляров. Эффективная обменная поверхность капилляров составляет в сумме примерно 1000 м2. Плотность капилляров в различных органах не одинакова. Она больше "средней" (усредненной) величины в 4-5 раз в головном мозге, миокарде, почках. Это значит, что при нарушениях микроциркуляции в жизненно важных органах вероятность возникновения их отека увеличивается. Относительно "средней" величины плотность капилляров меньше в костной, соединительной и жировой ткани.
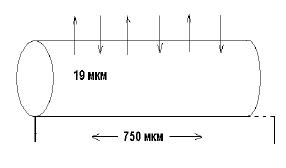
Функциональной или обменной единицей считается совокупность сосудов от артериол до венул. Общая длина функциональной единицы составляет примерно 750 мкм.
Различают 3 типа капилляров:
1 тип. С непрерывной стенкой. Образованы слоем эндотелиальных клеток, в мембранах которых имеются мельчайшие поры диаметром 4-5 нм. Этот тип капилляров преобладает в сосудах легких, мышечной, соединительной и жировой ткани.
2 тип. С фенестрированной стенкой. Между эндотелиальными клетками имеются фенестры - "окошки" диаметром 0,1 мкм. Часто фенестры прикрыты тончайшей мембраной ("окошки застеклены"). Этот тип капилляров преобладает в слизистой кишечника, клубочках почек (где осуществляется фильтрация).
3 тип. С прерывистой стенкой, в которой эндотелиальные клетки, прерываясь, образуют просветы. Через просветы могут проходить даже клетки крови. Этот тип капилляров имеется в синусоидах печени, селезенки, костном мозге.
 Рисунок
5.
Схема капилляра
Рисунок
5.
Схема капилляра
Кроме того, крупные молекулы могут переноситься через капиллярную стенку путем пино- и эмиоцитоза. Подошедшую молекулу эндотелиальная клетка "обнимает", поглощает в протоплазму (пиноцитоз) и, переместив к другой части клетки "выталкивает" (эмиоцитоз). Обмен в капиллярах осуществляется в основном благодаря диффузии, а также фильтрации и реабсорбции.
Диффузия в капиллярах описывается уравнением Фика. Скорость диффузии очень велика. При движении по функциональной единице капилляра жидкость плазмы успевает 40 раз обменяться с жидкостью межклеточного пространства. Иными словами при общей длине функциональной единицы капилляра в 750 мкм (/40) через каждые примерно 19 мкм стоит как "регулировщик движения" закон Фика, который меняет вектор направления жидкости то в одну, то в противоположную сторону.
Благодаря этому происходит непрерывный обмен жидкостей. Через общую эффективную обменную поверхность перемешивается таким образом 60 л. жидкости в минуту, 85000 л. жидкости в сутки (85000 примерно 85000 кг., 85 тонн!).
Фильтрация и реабсорбция в капиллярах описывается уравнением Старлинга. Их интенсивность определяется гидростатическим давлением в капилляре (Ргк), гидростатическим давлением в тканевой жидкости (Ргт), онкотическим давлением плазмы в капилляре (Рок), онкотическим давлением в тканевой жидкости (Рот) и коэффициентом фильтрации (К). К - соответствует проницаемости капиллярной стенки для изотонических растворов: 1 мл жидкости в 1 мин. на 100 г. ткани при Т 37оС:
В норме во всех капиллярах скорость фильтрации составляет примерно 14 мл/мин или 20 л/сут; скорость реабсорбции составляет примерно 12,5 мл/мин или 18 л/сут. Около 2 л/сут оттекает из интерстициального пространства по лимфатическим сосудам и впадает в правое предсердие, дополняя таким образом объем жидкости в сосудистом русле.
На сегодня физиологи пересматривают вышеизложенный механизм транскапиллярного обмена. Возможно, что в норме нет ни интенсивной фильтрации, ни интенсивной абсорбции воды и обмен ионами и метаболитами осуществляется за счет концентрационной разницы. Фильтрация или абсорбция - только медленно стабилизирующие или аварийный механизм, срабатывающий только при изменении осмолярности или кровопотере, и возможный объем аварийного обмена в единицу времени неизвестен.
Реология крови
Кроме перечисленных законов, которым подчиняется движение крови по сосудам, оно подчиняется также законам реологии. Реология - это наука о течении и деформациях. Она рассматривает механическое поведение различных материалов, если в процессе течения и деформации материал проявляет не менее двух из трех основных свойств: вязкость (свойство обратное текучести), пластичность, упругость. В реологии гемореология представляется как частный
вариант реологии.
Кровь обладает по меньшей мере двумя свойствами: вязкостью и пластичностью. Поэтому кровь относят к нелинейно-вязкопластичной среде. Это означает, что главной особенностью такой среды является сочетание переменной вязкости с пластичностью. При этом переменная вязкость зависит от скорости деформации (скорости течения жидкости). Вязкость - это свойство жидкости, сдерживающее ее течение или перемещение.
Таким образом, реологические свойства крови обусловлены тремя главными показателями: вязкостью крови, количеством частиц в крови (форменных элементов, крупных молекул) и скоростью потока крови.
На реологические свойства крови влияют многие факторы:
- Внешней среды (главный - температура): при ↑ Т - вязкость крови и плазмы ↓.
- Взаимодействие (главный - скорость кровотока): при↓ V - вязкость крови ↑, способность к агрегации ↑.
- Плазменные:
↑ гамма-глобулина, фибриногена, жирных кислот, триглицеридов, холестерина - ↑ вязкость крови.
- рН крови независимо от направления - ↑ вязкость крови (ацидоз - разбухание, алкалоз - сморщивание эритроцитов).
Под синдромом повышенной вязкости принято понимать комплекс изменений реологических свойств крови. Комплекс изменений составляют:
1) повышение вязкости плазмы и крови (косвенно - время свёртываемости крови);
2) увеличение гематокрита (Ht);
3) усиление склонности к агрегации (косвенно СОЭ);
4) уменьшение пластичности (или деформируемости) эритроцитов (косвенно pH),
5) увеличение концентрации фибриногена.
Гемодилюция
Иногда с целью улучшения микроциркуляции приходиться разбавлять кровь. А.Н. Филатовым и Ф.В. Баллюзеком (1972) установлено, что при патологических состояниях, требующих гемодилюции, наиболее оптимальным является разбавление (или разведение) крови на 30 %, что случайно совпадает с гематокритом 30-31 %.
При большем разведении и хорошей скорости потока увеличивается вероятность перехода ламинарного потока в турбулентный вследствие "кувыркания" форменных элементов и крупных частиц крови. Кроме того, избыточная гемодилюция изменяет концентрацию факторов свёртывающей системы крови, что опасно повышенной кровоточивостью.
Регуляция кровообращения
