
книги2 / monograph_1
.pdfкоторые также использовались в качестве источника углерода во вспучивающейся огнезащитной системе. Показано, что оба растительных продукта могут эффективно улучшать огнезащитные свойства вспучивающейся системы.
Очевидно,чтобольшинствобытовыхотходовмогутбытьиспользованы в качестве источника углерода для вспучивающейся огнезащитной системы из-за структуры, богатой OH-группами. Все эти работы, упомянутые выше, прокладывают новый путь к повторному использованию бытовых отходов, что способствует устойчивому развитию общества и повышает пожаробезопасность полимеров.
Существует два типа растительных отходов, целлюлозные нановолокна и лигнин, которые часто применяются в огнестойких полимерных материалах из-за возобновляемых, биоразлагаемых и нетоксичных свойств. Как целлюлозные нановолокна, так и лигнин имеют структуру, богатую OH/C, которая может служить в качестве обугливающего агента во время горения, и их огнестойкие свойства могут быть дополнительно улучшены путём химического введения различных огнестойких групп, например,
содержащих: P, N и Si (Yang et al., 2021).
ГЛАВА 3. ИСТОЧНИКИ И ПУТИ ПОПАДАНИЯ БРОМИРОВАННЫХ АНТИПИРЕНОВ
ВОКРУЖАЮЩУЮ СРЕДУ И ЧЕЛОВЕКА
3.1.Бромированные антипирены в окружающей среде, их абиотическая и биотическая деградация
В середине 20-го века произошёл бурный рост индустрии пластмасс. Во многих домах сегодня есть пластиковый сайдинг и обшивка, пенополиуретановый утеплитель. Во многих жилых домах есть водопроводные и канализационные трубы из поливинилхлорида и километры электрических кабелей, многие из которых имеют пластиковую обшивку. Мебель и текстиль часто содержат полимеры, в том числе, шторы и обои, пенополи-
51

уретановые диваны, постельное бельё, подушки и многие виды одежды. В настоящее время в большинстве домов имеется разнообразная коллекция электроники, в том числе из поликарбоната и полистирола: компьютеры, планшеты, телефоны, игровые приставки, телевизоры, аккумуляторы и силовые трансформаторы.
Производители пластиков стремились к созданию недорогих, прочных, лёгких и пластичных изделий, защищённых от возгорания (рис. 8). Однако производители не предвидели, как их изобретения изменят химический состав окружающей среды и, что более важно, повлияют на биохимическую и гормональную активность человеческого организма.
Рисунок 8. Продукты и изделия, содержащие ПБДЭ
Антипиренынетестировалисьнавозможностьихперемещений по воздуху, воде, океанам или почве. Возможно, потому, что промышленность не могла предсказать величину и разнообразие их будущего использования в десятках тысяч потребительских товаров.
Потенциальными путями попадания бромированных антипиренов в окружающую среду являются: сжигание мусора, сточ-
52
ные воды, выщелачивание со свалок и улетучивание из электрическихкомпонентоввпроцессеихиспользования(Darnerudetal., 2001). Источники бромированных антипиренов также включают промышленныеобъекты,которыепроизводятбромированныеантипирены, а также предприятия, использующие бромированные антипирены в широком спектре потребительских товаров.
ПБДЭ,ГБЦДДиПБДпредставляютсобойдобавки,смешанные с полимерами и химически не связанные c пластиком или текстилем. Поэтому они могут отделяться или выщелачиваться с поверхности товаров и оборудования в окружающую среду. TББФ A химически связан с материалом, но, не полимеризуясь, он может попадать в окружающую среду (de Wit, 2002). Данные об уровнях TББФ A в биоте очень ограничены, что, возможно, связано с коротким периодом полураспада в окружающей среде. TББФ A обнаружен в осадке сточных вод, донных отложениях и почве.
По данным Environmental Protection Agency (USEPA) (2005),
пути, по которым ПБДЭ попадают в окружающую среду, предположительно, могут включать выбросы при производстве или переработке таких продуктов, как пластик или текстиль, при старении и износе потребительских товаров, а также прямое воздействие во время использования (например, от мебели).
Атмосферные выбросы ПБДЭ значительно больше, чем выбросы в почву и воду (Earnshaw et al., 2013). При этом концентрации ПБДЭ, связанных с частицами, внутри помещений выше, чем концентрации в воздухе снаружи. Суммарные концентрации ПБДЭ в воздухе варьируют от 5,5 пг/м3 в сельской местности до 52 пг/м3 в городском воздухе.
В исследовании авторов (Wu et al., 2014) применялся метод длительного отбора проб дымовых газов электродуговой печи (до168часов),называемыйадсорбционнымметодомотборапроб диоксиновифуранов(AMESA).Былопоказано,чтоПХБиПБДЭ являются наиболее распространёнными загрязнителями в дымовых газах электродуговой печи, и их концентрации на один-три порядка выше, чем других СОЗ.
53
У ряда исследователей возникли серьёзные опасения, что при попадании ПБДЭ в окружающую среду, помимо биоаккумуляции, возможно преобразование ПБДЭ под воздействием УФизлучения. Исследователями было показано, что фотодебромирование представляет собой ступенчатый процесс(Linget al.,2019), который, по-видимому, нелегко объяснить с точки зрения взаимной ориентации брома в орто-, мета- и пара-положениях в соответствующих ароматических кольцах (Wang et al., 2018). В работе авторов сообщалось, что лёгкость реакций фотодебромирования в полибромированных ароматических соединениях с наибольшим числом атомов брома определяется наибольшим растяжением связи C–Br в исходном возбуждённом состоянии, указывая на то, что возбуждения бромированных антипиренов происходят через π→π*, или π→σ*, или n→σ* электронные переходы (Saeed et al., 2020). Не в последнюю очередь влияет эффект полностью бромированного ароматического кольца, что создаёт стерический запирающий эффект между соседними атомами брома, тем самым затрудняя первые этапы дебромирования. В то время как УФ-разложение бромсодержащих антипиренов, таких как де- ка-БДЭ, привлекло пристальное внимание, УФ-разложение декабромдифенил этана или 1,2-бис(пентабромфенил) этана изучено меньше. L. Najia с коллегами (2014) показали, что Saytex 8010 может фотолитически подвергаться эффективному ступенчатому восстановлению, дебромированию, которое следует кинетике первогопорядка.ПриУФ-облучениибромированногополистиро- лаобразуется75различныхпродуктовразложения,втовремякак его термическое разложение приводит к образованию значительно меньшего числа метаболитов (Koch et al., 2019).
В исследовании (Lörchner et al., 2019) был проведён прямой и непрямой фотолиз нового бромированного антипирена
2,4,6-трис(2,4,6-трибромфенокси)-1,3,5-триазина (TTBP-TAZ)
в смеси органических растворителей в условиях УФ-света и имитации солнечного облучения, и впервые идентифицированы образующиеся продукты фотопревращения. Показано, что TTBP-TAZ почти полностью разложился в течение 10 мин
54
под действием УФ-облучения. Из-за быстрой деградации нельзя было наблюдать какой-либо определённый кинетический порядок. Реакция при моделировании солнечного облучения была намного медленнее, и, таким образом, можно было определить кинетику первого порядка. Наблюдаемая константа скорости фотолиза (k), а также период полураспада T1/2 были оценены как: k=(0,0163±0,0002)ч-1 иT1/2=42,3чсоответственно.Добавление
2-пропанола и перекиси водорода при исследовании влияния непрямого фотолиза под действием УФ-облучения не оказало влияния на разложение TTBP-TAZ. Тем не менее, удаление TTBPTAZ под действием УФ-света и искусственного солнечного света без дополнительных химикатов (кроме растворителя) указывает на то, что прямой фотолиз играет значительную роль в механизме деградации TTBP-TAZ. В обоих экспериментах по облучению при деградации TTBP-TAZ образовались ранее не изученные метаболиты. В целом, два основных метаболита были определены при УФ-облучении и восемь последовательных продуктов дебромирования наблюдались при облучении искусственным солнечным светом. Их определяли с помощью ВЭЖХ и МС соответственно. На основе проведённых экспериментов сделаны выводы об основных путях разложения TTBP-TAZ: последовательное дебромирование, а также фото-перегруппировка Фриса.
Широкое использование ГБД в качестве огнеупорной добавки ввиду высокой химической стабильности привело к загрязнению окружающей среды. Деградация ГБД в воде практически отсутствует (LD50 > 2 мес.), высокая персистентность в почве и отложениях (LD50 > 6 мес.). Деградация ПБД в результате чисто абиотических химических реакций (за исключением фотохимических) считается маловероятной. Процесс разложения ГБД в окружающейсредеопределяетсяеговысокимизначениямиKow(6,39)ималой растворимостью в воде (3 мкг/л), в результате чего происходит его сорбция на твёрдых частицах (пыль, почва и отложения) и органических веществах. Хотя ГБД менее летуч, чем любой из СОЗ, вероятен его перенос с загрязнёнными частицами на большие расстояния (обнаружен в живых организмах, обитающих в Арктике).
55
Перенос ГБЦДД на большие расстояния регулируется переносом аэрозолей и частиц, которые поглощают его вследствие низкой летучести. ГБЦДД отличается стойкостью в атмосфере, где период его полураспада превышает двое суток. Был смоделирован период полураспада ГБЦДД в атмосфере в результате реакции в газовой фазе с гидроксильными радикалами (OH*), полученное расчётное значение составило 3,2 сут.
Физико-химическиесвойстваГБЦДДтаковы,чтосуществует возможность активного обмена между поверхностью земли и атмосферой в результате сезонных и суточных колебаний температур, что создаёт возможность для переноса ГБЦДД на большие расстояния вследствие ряда скачков осаждения/испарения («эффект кузнечика»). В снежном покрове наблюдаются пики концентраций ГБЦДД зимой, что обусловлено более высокой способностью снега к очищению воздуха, по сравнению с дождём, а также более высокой концентрацией частиц в зимний период.
Биодеградация двух основных изомерных форм ГБЦДД в почве составляет 5–6%. Скорость деградации ГБЦДД в присутствии кислорода замедляется. Полураспад в аэробных отложениях при 20 °C составляет соответственно для α-, β- и γ-ГБЦДД: 113, 68 и 104 сут. Основным продуктом трансформации является 1,5,9-циклододекатриен, который образуется в результате поэтапного восстановительного дегалогенирования ГБЦДД.
Было установлено, что разложение дека-БДЭ до токсичных метаболитов окта- и пента-БДЭ наблюдается в осадке сточных вод в течение двух лет (Gerecke et al., 2006). Реакции дебромирования имеют особое значение в биоразложении как дека-БДЭ, так и ГБЦДД и, скорее всего, происходят как в анаэробных, так и в аэробных условиях. Однако, помимо различий в прочности связи C–Br, характер реакций дебромирования в целом отличается. Это связано с тем, что удаление брома из полиароматической структуры, такой как дека-БДЭ, будет по существу восстановлением свободных ионов Br, тогда как в случае алифатического ГБЦДД будет происходить дегидробромирование, ведущее к образованию ненасыщенных производных циклододецена. ГБЦДД
56
технической чистоты включает три хиральных диастереомера, каждый из которых существует в виде пары энантиомеров
(European Union RiskAssessment, 2008), влияющих на пути дегра-
дации. Исследования J.W. Davies с коллегами (2005) биодеградации технических смесей ГБЦДД в почвах и пресноводных отложениях показали, что для γ-ГБЦДД не были идентифицированы бромированные продукты разложения, и биоразложения минорных α- и β-диастереомеров также не наблюдалось. Дальнейшие исследования осадка и отложений сточных вод выявили тетрабромциклододецен,дибромциклододекадиенициклододекатриен
вкачестве метаболитов всех трёх диастереоизомеров (Davis et al., 2006). В исследовании T.H. Chang с коллегами (2020) отмечено, что оптимальная биодеградация ГБЦДД происходила под действием микробных штаммов Rhodopseudomonas palustris, выделенных из почвы рисовых полей, при нейтральном значении рН и при 35 °С. Мольные соотношения высвобождённых бромид-и- онов наблюдались в диапазоне от 1 до 3,5, что свидетельствует о протекании реакций дебромирования с одновременным производством двух метаболитов: пентабромциклододеканола и пентабромциклододецена. Присутствие ионов металлов также оказало значительное влияние на биоразложение ГБЦДД. Как было показано D. Li с коллегами (2016), сульфид железа (II), который часто находится в анаэробных отложениях, ускоряет восстановительное последовательное дибромэлиминирование ГБЦДД с образованием 1,5,9-циклододекатриена, что предполагает его использование в качестве реактивного агента для обработки отложений, загрязнённых ГБЦДД.
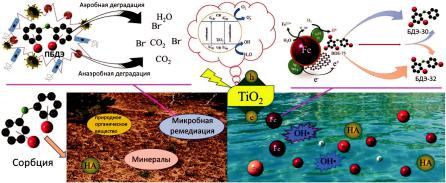
На рисунке 9 отображены процессы, происходящие с ПБДЭ
вокружающей среде (Sahu et al., 2021).
Исследователи (Chou et al., 2016) изучили биоремедиацию дека-БДЭ (25 мг/кг) с использованием почвенно-водных микроценозов в лабораторных условиях Установлено, что эффективная биодеградация дека-БДЭ происходила во всех микроценозах. Были идентифицированы различные биометаболиты, а именно: конгенеры ПБДЭ и гидроксилированный БДЭ. Также были об-
57
наружены продукты восстановительного дебромирования, такие как, конгенеры три-БДЭ и гепта-БДЭ, и их суммарная концентрация колебалась от 77,83 до 91,07 нг/г. Предполагается, что механизм биодеградации дека-БДЭ в почвенно-водных микроценозах состоит из ряда биологических реакций, включающих гидроксилирование и дебромирование.
Рисунок 9. Процессы, происходящие с ПБДЭ в окружающей среде
(по Sahu et al., 2021)
В ходе биодеградации дека-БДЭ были идентифицированы ферментыкатехол2,3-оксигеназы,которыеспособныкатализиро- вать мета-расщепление в определённых небромированных участках углеродных скелетов. Никакого очевидного влияния на функциональное разнообразие сообществ не наблюдалось во время биодеградации дека-БДЭ. В различных почвенно-водных микроценозах был идентифицирован микроорганизм Pseudomonas sp.
вкачестве одного из основных видов факультативных бактерий (99% гомологии). Эти результаты могут стать основой для разработки системы микробной ремедиации дека-БДЭ. Бактериальная смешанная культура может быть выбрана для биоремедиации де- ка-БДЭ в условиях in situ. Система почвенно-водного микроценоза может быть успешно применена для проведения работ ex situ.
Для разложения декабромдифенилового эфира (БДЭ-209)
всуспензияхглиныавторы(Changetal.,2021)использовалисоче-
58
тание УФ-фотолиза и биодеградации. В экспериментах использо- валибиореакторсбиосуспензией,вкоторомразложениеБДЭ-209 было максимальным за счёт одновременного применения светодиодного УФ-облучения и биодеградации смешанной бактериальной культурой. Скорость разложения БДЭ-209 уменьшалась
вследующем порядке: комбинация УФ-фотолиз-биодеградация (1,31×10-2 сут-1) > только УФ-фотолиз (1,10×10-2 сут-1) > только биодеградация (1,00×10-2 сут-1). Обнаруженные промежуточные продукты разложения включали гидроксилированные ПБДЭ, частично дебромированные конгенеры ПБДЭ и полибромированный дибензофуран. Выделены штаммы бактерий, устойчивые к УФ-излучению, которые могут утилизировать БДЭ-209 в качестве единственного источника углерода: Stenotrophomonas sp., Pseudomonas sp. и Microbacterium sp. Эти штаммы несут важные функциональные гены, кодирующие диоксигеназы и восстановительные дегалогеназы.
Авторы изучили и сравнили разложение ТББФ А, ГБЦДД идека-БДЭванаэробныхусловияхвсброженномосадкесточных вод (Gerecke et al., 2006). Периоды полураспада ТББФ А и технической смеси ГБЦДД составили 0,59 и 0,66 сут. соответственно. Тот факт, что период полураспада (±)-α-ГБЦДД был почти в два раза выше по сравнению с (±)-β-ГБЦДД и (±)-γ-ГБЦДД, является важным результатом в связи с обсуждением стойкости отдельных стереоизомеров ГБЦДД и сообщениях об относительно высоком содержании α-ГБЦДД в биоте. Периоды полураспада ТББФ А и технической смеси ГБЦДД не зависели от наличия дополнительных питательных веществ или праймеров. Концентрации ТББФ А и технической смеси ГБЦДД снижались и в стерильных контрольныхобразцах,нов50размедленнее,чемприинкубации
внестерильных условиях. По сравнению с ТББФ А и технической смесью ГБЦДД дека-БДЭ продемонстрировал гораздо более длительный период полураспада, составляющий 7×102 сут. в тех же условиях. Константы скорости разложения псевдопервого порядка уменьшались в ряду: ТББФА (±)-γ-ГБЦД (±)-β-ГБЦД >
(±)-α-ГБЦД дека-БДЭ.Предварительныеисследованияучёных
59
показали, что разложение ТББФ А, ГБЦДД и дека-БДЭ происходит аналогичным образом в промышленных анаэробных метанотенках.
DBNPG представляет собой бромированный антипирен, который используется в качестве добавки при производстве пластиковых полимеров и в качестве промежуточного химического вещества для других антипиренов. Он классифицируется как трудно биоразлагаемый, с периодом полураспада более 100 лет,
ина основании экспериментальных исследований на животных считается канцерогеном. Исследователи (Segev et al., 2007) впервые продемонстрировали полную биодеградацию DBNPG в аэробных условиях. Анализ общего органического углерода указывал на полную минерализацию DBNPG. Биодеградация данного антипирена сопровождалась выделением в среду бромида, вероятно, за счёт биологической реакции дебромирования бактериальными консорциумами. Было обнаружено, что в этот процесс вовлечено не менее семи видов бактерий, среди которых есть виды, сходные со штаммами, известными своей дегалогенирующей способностью.
Пента-БДЭ попадает в окружающую среду в процессе производства и использования продукции, а также после её удаленияввидеотходов(разборкаиповторноеиспользованиебытовой электроники и электробытовых приборов, переработка отходов с целью извлечения ценных металлов и дальнейшая торговля). В Северной Америке и Западной Европе пента-БДЭ содержится в основном в пенополиуретане, использовавшемся при изготовлении мебели для дома и для учреждений. Потенциальными «очагами» выброса пента-БДЭ в морскую среду являются некоторые развивающиеся страны.
Проблемой считается выявление и обработка оборудования
иотходов,содержащихПБДЭ.Внекоторыхстранахиспользованные материалы, содержащие такие вещества, как пента-БДЭ, рассматриваются как опасные отходы. Отходы, образующиеся при производстве строительных материалов, тканей и мебели, вывозятся на свалки или сжигаются. Чаще всего материалы, в кото-
60
