
Uchebnoe_posobie
.pdfУ пациента с пневмонией содержание С-реактивного белка в крови составляло 52 мг/л. Через 48 часов после назначения антибиотикотерапии содержание С-реактивного белка в крови снизилось до 39 мг/л (аналитическая вариабельность – 8 мг/л, биологическая – 5 мг/л).
Вопрос. Продолжать начатую антибиотикотерапию или произвести замену на антибиотик резерва?
Задача 1.3
У пациента с циррозом печени содержание билирубина в крови составляло 42 мкмоль/л. Через 6 месяцев после назначения гепатопротектора содержание билирубина в крови снизилось до 37 мкмоль/л (аналитическая вариабельность – 4 мкмоль/л, биологическая – 2 мкмоль/л).
Вопрос. Продолжать ли начатую терапию гепатопротектором или произвести его замену на другой гепатопротектор?
Задача 1.4
В лаборатории № 1 повышение ТТГ выявлено у 838 человек из 1016 больных с первичным гипотиреозом, показатели ТТГ находились в пределах референтного интервала у 59 человек из 72 здоровых обследованных. В лаборатории № 2 повышение ТТГ выявлено у 193 человек из 254 больных с первичным гипотиреозом, показатели ТТГ находились в пределах референтного интервала у 212 человек из 285 здоровых обследованных.
Вопрос. Какую лабораторию выбрать для проведения скрининга на врожденный гипотиреоз?
Задача 1.5
На профилактическом приеме у трех пациентов выявлен множественный кариес. После направления проб слюны этих пациентов для анализа в биохимическую лабораторию он выявил у всех трех пациентов снижения уровня кальция в нестимулированной слюне до 15 мкг/мл (норма – 37 мкг /мл), в связи с чем после проведения санации ротовой полости в комплексном лечении были назначены:
1-му пациенту паста с кальцием,
2-му пероральные таблетированные препараты кальция,
3-му порошок из яичной скорлупы.
Через месяц стоматолог произвел контрольный забор слюны у всех трех пациентов и направил ее на биохимическое мониторинговое исследование:
у1-го пациента содержание кальция в слюне 30 мкг/мл (аналитическая вариабельность – 3 мкг/мл, биологическая – 4 мкг/мл),
у2-го пациента содержание кальция в слюне 32 мкг/мл (аналитическая вариабельность – 5 мкг/мл, биологическая – 4 мкг/мл),
у3-го пациента содержание кальция в слюне 27 мкг/мл (аналитическая вариабельность – 3 мкг/мл, биологическая – 2 мкг/мл).
Вопрос. Оценить при помощи биохимического мониторинга содержания кальция в слюне необходимость продолжения профилактического лечения у каждого из пациентов.
Задача 1.6
В лаборатории № 1 повышение глюкозы выявлено у 1108 человек из 1262 больных с сахарным диабетом, показатели глюкозы находились в пределах референтного интервала у114 человек из 168 здоровых обследованных. В лаборатории № 2 повышение глюкозы выявлено у 394 человек из 429 больных с сахарным диабетом, показатели глюкозы находились в пределах референтного интервала у 27 человек из 34 здоровых обследованных.
Вопрос. Какую лабораторию выбрать для проведения скрининга на сахарный диабет?
11
Занятие 2. Патобиохимия эндогенной интоксикации как типового патологического процесса, значение ее своевременной диагностики в клинике
Цель занятия. Познакомить студентов с биохимическими основами эндогенной интоксикации при некоторых патологических состояниях, дать представление о молекулах средней и низкой молекулярной массы (МСиНМ) как материальном субстрате эндогенной интоксикации, обосновать целесообразность различных методов биохимического обследования больных для оценки тяжести эндогенной интоксикации и эффективности дезинтоксикационной терапии.
I. Внеаудиторная самостоятельная работа студентов.
1. Цель самоподготовки. После самостоятельного изучения материала студент должен знать: основные пути обмена белков и липидов, дезинтоксикационная функция печени, основные функции белков сыворотки крови, биологические функции лизосом и микросом, представление о бактериальных токсинах.
2. Задание для самоподготовки:
А) знать основные клинические проявления эндогенной интоксикации у больного в условиях клиники.
Б) изучить метаболические основы эндогенной интоксикации при критических состояниях и некоторых хронических патологических состояниях.
В) Биохимические методы оценки тяжести эндогенной интоксикации и эффективности дезинтоксикационной терапии.
Г) изучить материалы лекционного курса, основной и дополнительной литературы, уделив особое внимание следующим основным вопросам темы:
1.представление о молекулах средней и низкой молекулярной массы;
2.понятие об организации функциональной системы детоксикации в организме;
3.принципы нейтрализации и выделения эндогенных токсических субстанций в зависимости от механизма образования, молекулярной массы и физико-химических свойств;
4.стадийность развития эндотоксикоза, показатели лабораторных исследований в соответствии со стадиями;
5.знать способы диагностики эндогенной интоксикации, применяемые в клинике.
3. Содержание практического занятия:
Основные клинические проявления эндогенной интоксикации. Эндотоксикоз (ЭТ) - представляет собой типовой патологический процесс, являющийся структурно-функциональным ответом организма на токсическую агрессию как эндогенной, так и экзогенной природы, его можно
12
охарактеризовать как клиническое проявление эндогенной интоксикации, которая не сдерживается механизмами адаптации и компенсации токсической информации.
Клинические проявления многообразны: гипертермия, нарушение функции центральной нервной системы (ЦНС), сердечно-сосудистой системы, печени, почек, иммунокомпетентных органов и системы кроветворения. Такой полиморфизм проявлений, с одной стороны, облегчает постановку диагноза, с другой, нередко затрудняет его с точки зрения выявления ведущих симптомов основного заболевания.
С нормализацией кровообращения после травматического или ожогового шока создаются условия для быстрого всасывания разнообразных продуктов из очага поражения. Такие же явления отмечаются и при некротических и гнойнонекротических процессах, что связано со значительным повышением капиллярной проницаемости, обеспечивающей быстрое распространение токсических веществ в организме. Токсичность продуктов и их количество существенно зависят от величины некроза и его характера — она всегда выше при наличии влажного некроза. Кроме гистиогенных факторов важная роль в развитии интоксикационного синдрома принадлежит бактериальному фактору. Источником инфицирования может быть микрофлора собственной нормальной кожи, верхних дыхательных путей и экзогенная микрофлора больничной палаты.
При разрушении микроорганизмов в крови высвобождаются продукты их распада и пирогены, прежде всего, липополисахаридные комплексы, определяющие развитие лихорадки, усиливающие синдром интоксикации, активирующие траскрипционные факторы, влияющие на адгезивные свойства клеток крови и эндотелия.
Клинически нарушение функции ЦНС может проявляться в психомоторном возбуждении, дезориентации во времени слуховых и зрительных галлюцинациях, спутанности сознания, бреде.
Со стороны сердечно-сосудистой системы чаще всего отмечается выраженная тахикардия иногда с болевым синдромом, нередко развитие токсического миокардита. При выраженной интоксикации страдают и процессы микроциркуляции со значительным увеличением проницаемости микроциркуляторного русла.
Частое проявление эндогенной интоксикации — развитие токсического гепатита и почечной недостаточности. Кроме того, возможны развитие анемии и иммунодепрессивных состояний, что может привести к септическим осложнениям.
Развитие эндогенной интоксикации во многом определяется изменениями метаболизма в ответ на травму или некротический процесс в органах и тканях.
Хотя эндогенная интоксикация полиэтиологична, можно выделить следующие основные первичные механизмы ее развития:
продукционный или обменный, обусловленный избыточной продукцией эндогенных токсических субстанций (разлитой перитонит, острый панкреатит, острая пневмония);
13
резорбционный, когда происходит резорбция токсических веществ из ограниченного очага инфекции, распадающихся тканей (кишечная непроходимость, флегмоны мягких тканей, абсцессы и т.д.);
реперфузионный, при котором в системный кровоток поступают вещества, накопившиеся в длительно ишемизированных тканях, а также выделившиеся из клеток этих тканей при их повреждении активными формами кислорода и избытком свободных радикалов на фоне несостоятельности системы антиоксидантной защиты (шок, реперфузионный синдром, операции с применением аппарата искусственного кровообращения и т.д.);
ретенционный, при котором накопление эндотоксических субстанций (ЭТС) происходит в результате нарушения их выведения естественными органами детоксикации (острая почечная и печеночная недостаточность);
инфекционный, в результате поступления микроорганизмов, продуктов их обмена и распада из очага инвазивной инфекции или путем транслокации из извращенно контаминированного желудочно-кишечного тракта.
Вразвитии острого эндотоксикоза одновременно или последовательно могут участвовать несколько механизмов образования ЭТС и накопления их во внутренней среде организма.
Острый ЭТ протекает как каскадный процесс. Развитие и прогрессирование его связано с несоответствием между образованием (поступлением и т.д.) токсических субстанций, в том числе образующихся в результате последующей вторичной токсической аутоагрессии, и способностью органов, входящих в функциональную систему детоксикации (легкие, печень, почки, желудочно-кишечного тракта (ЖКТ), кожа, система иммунологического надзора), их трансформировать, нейтрализовать и элиминировать. Существенное значение могут иметь нарушения соотношений между веществами антагонистами в гуморальных регуляторных системах (ферментыантиферменты, оксиданты-антиоксиданты, цитокины-антицитокины, коагулянты-антикоагулянты и т. д.).
Исходя из взаимоотношений эндогенной интоксикации и возможностей функциональной системы детоксикации (ФСД) можно выделить 4 стадии развития эндотоксикоза:
в стадии компенсации ФСД полностью компенсирует токсемическую нагрузку;
в стадии напряжения скорость наработки токсических субстанций совпадает
смаксимальными возможностями ФСД;
в стадии субкомпенсации поступление токсических субстанций определенно превышает возможности ФСД;
и, наконец, в стадии декомпенсации развивается несостоятельность органов ФСД и появляются жизнеугрожающие метаболические и функциональные нарушения.
Основные метаболические синдромы эндогенной интоксикации во многом совпадают с наблюдающимися при термических ожогах. Однако степень их выраженности и значимость в определении тяжести состояния имеет ряд особенностей. Это, прежде всего, связано с характером соединений, которыми непосредственно или косвенно определяются морфофункциональные
14
проявления интоксикации, а также теми процессами, которые приводят к их образованию.
Кпроцессам, ведущим к образованию токсических соединений, относится гипоксия и связанная с ней активация перекисного окисления липидов (ПОЛ), тканевой протеолиз с образованием промежуточных и конечных продуктов, нарушение процессов гемостаза с развитием ДВСсиндрома. Важную роль в развитии синдрома эндогенной интоксикации играет изменение комплексообразующих свойств белков сыворотки крови, белковообразовательной и дезинтоксикационной функции печени, ее микросомального аппарата, обеспечивающего деградацию и окисление различных токсических продуктов и ксенобиотиков.
Ктоксинам гистиогенной природы обычно относят биогенные амины — продукты активного протеолиза и декарбоксилирования аминокислот, аммиак, фенолы, сложные белки (глико- и липопротеиды), перекисные соединения и некоторые простагландины. В последнее время особенное значение придается МСиНМ и некоторым фракциям белков крови — альфа-глобулинам, модифицирующим биологическую активность МСиНМ, а также обладающих антиоксидантной активностью за счет церулоплазмина, транспортного белка относящегося к этой фракции.
МСиНМ как высокоактивные биологические соединения в определенных, очень незначительных количествах присутствуют в тканях и крови здорового человека, выполняя регуляторные функции по отношению к различным системам организма (сердечно-сосудистой, нервной, иммунной, кроветворения
игемостаза). Однако при различных патологических состояниях в результате активного протеолиза количество молекул средней массы существенно возрастает, кроме того, появляются пептиды (среднемолекулярные пептиды), обладающие токсическим действием. Эти пептиды проявляют отрицательное хроно- и инотропное действие на миокард, нарушают процессы микроциркуляции, повышают проницаемость гематоэнцефалического барьера, подавляют иммунологические процессы.
Функции и количество МСиНМ регулируется очень сложной системой, в которую входит большое число компонентов, в том числе ферменты протеолиза, форменные элементы крови на чьих мембранах сорбируются МСиНМ, белки крови (в основном альфа-глобулины), модифицирующие их действие. В условиях повышенного протеолиза эта система полностью не срабатывает, в результате чего значительная часть МСиНМ в свободном состоянии проявляет свое отрицательное действие
В связи с этим успешное практическое применение нашло назначение больным ингибиторов протеиназ, переливание отмытых эритроцитов и внутривенное введение белковых препаратов. С целью активной дезинтоксикационной терапии широко применяются стимулированный диурез, а также экстракорпоральные методы (гемо- и лимфосорбция, плазмаферез, ультрафильтрация, непрямое электрохимическое окисление крови натрия гипохлоритом и др.).
С учетом повышенных процессов ПОЛ в клинической практике применяют естественный липофильный антиоксидант токоферол стабилизирующий клеточные мембраны, уменьшающий лабилизацию лизосом,
15
улучшающий функцию микросомальных ферментов, а также аскорбиновую кислоту, как фактор регенерации токоферола.
Биохимические методы оценки тяжести эндогенной интоксикации и эффективности дезинтоксикационной терапии
Можно выделить лабораторные критерии нескольких уровней:
маркеры острого отравления или эндогенной интоксикации, если они четко очерчены в данной клинической ситуации;
лабораторные критерии, характеризующие вторичную токсическую аутоагрессию, ориентированные на оценку реакции организма данного больного на первичную и вторичную интоксикацию, а также позволяющие определять динамику токсичности компонентов внутренней среды и стадию ЭТ;
показатели, характеризующие работу ФСД, органов и систем
жизнеобеспечения организма.
Среди биохимических методов можно назвать исследование белкового спектра крови, содержание в крови мочевины и креатинина, функциональные пробы печени, активность протеаз, содержание в крови МСиНМ, интенсивность ПОЛ, активность моноамннооксидаз (МАО) и диаминооксидаз (ДАО) крови.
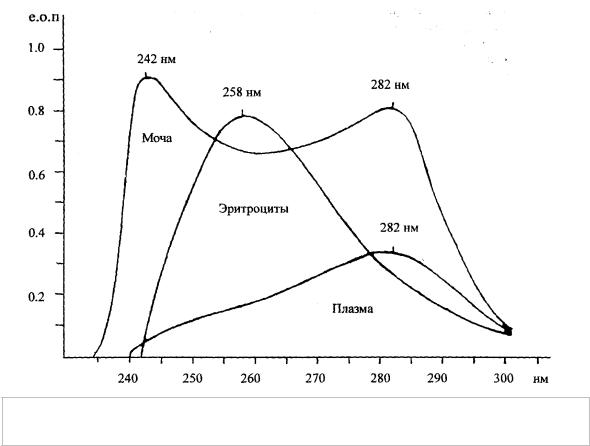
Рис. 2.1. Нормальные спектрограммы МСиНМ плазмы, эритроцитов и мочи
Считается, что основным токсическим субстратом, ответственным за возникновение стадии аутоагрессии эндотоксикоза, могут стать продукты клеточной дезорганизации, неполного распада и неферментного превращения белков крови и тканей. Они представлены в основном среднемолекулярными пептидами (СМП) с молекулярной массой 500—5000 Да. Наиболее точно
16
фракцию СМП можно выделить методами гель-хроматографии на носителях, методами жидкостной и газовой хроматографии, масс-спектрометрии или ультрафильтрации.
Отдельно следует сказать о применении для выявления СМП спектрофотометрических методов, например, методики определения молекул средней массы (МСМ) по Н. И. Габриэлян или методики определения молекул низкой и средней массы (МНиСМ) по М. Я. Малаховой.
На основании характера спектрограмм плазмы крови, эритроцитов и мочи в процессе развития и прогрессирования эндотоксикоза М.Я.Малахова выделяет 5 биохимических фаз эндогенной интоксикации:
в первой начальной фазе интоксикации наблюдается увеличение высоты эритроцитарного пика при неизмененной спектрограмме плазмы (компенсаторная фаза);
во второй фазе увеличивается концентрация метаболитов как в плазме, так и в эритроцитах (фаза накопления продуктов из очага агрессии);
для третьей фазы характерна стабилизация спектрограммы эритроцитов (полное насыщение) и дальнейшее увеличение высоты спектрограммы плазмы (фаза обратимой декомпенсации органов функциональной системы детоксикации);
для четвертой фазы свойственно снижение высоты эритроцитарного пика до нормы и ниже (вероятно, вследствие изменения структуры мембраны эритроцитов) и продолжающийся рост количества оптически активных веществ в плазме (фаза несостоятельности систем гомеостаза и необратимой декомпенсации функциональной системы детоксикации).
Довольно редко удается наблюдать пятую, терминальную стадию эндогенной интоксикации, когда отмечается значительное повреждение мембран, сопровождающееся снижением содержания метаболитов как на эритроцитах, так и в плазме крови (фаза полной дезинтеграции систем и органов). Нормальная спектрограмма имеет следующий вид.
Определение МСиНМ, например, при эндогенной интоксикации, вызванной термическими ожогами, высоко коррелирует как с тяжестью травмы (по индексу Франка), так и с другими показателями, отражающими тяжесть интоксикации – лейкоцитарным индексом интоксикации, индексом сдвига нейтрофилов, парамецийным тестом и др.
Широкое диагностическое значение приобрело определение активности ПОЛ. Процессы ПОЛ активируются при самых разнообразных патологических процессах, имея, таким образом, неспецифический характер. Исследование ПОЛ не может быть применено в целях дифференциальной диагностики, но для определения степени тяжести патологического процесса, в том числе и эндогенной интоксикации, оно используется весьма успешно. С этой целью применяются биохимические и биофизические методы, такие как хемилюминесцентный анализ, амперометрический анализ общей антиоксидантной активности биологических жидкостей, определение количества перекисных продуктов, реагирующих с тиобарбитуровой кислотой (ТБК-активные продукты в виде тиобарбитурового числа (ТБЧ)).
17
Специфичным для некоторых видов эндогенной интоксикации, в частности ожоговой, является показатель аминооксидазной активации крови. В норме МАО (субстрат бензиламин) равняется 16,2 ± 3,8 мкмоль/(л•ч), а ДАО (субстрат ксилилендиамин) — 0,8 ± 0,05 мкмоль/(л•ч).
При тяжелой эндогенной интоксикации активность МАО может снижаться до 3,5 ± 1,8 мкмоль/(л•ч), в то время как ДАО увеличивается до 17,5
± 1,6 мкмоль/(ч•л). Такие изменения очень характерны, что делает диагностически значимым коэффициент МАО/ДАО (в норме около 19, а при очень тяжелой ожоговой интоксикации может снижаться до 0,2).
Особенно информативна в этом отношении динамика ДАО-активности. При благоприятном течении ожоговой болезни активность ДАО постепенно нормализуется, в то время как при неблагоприятном исходе наблюдается повторный более выраженный рост активности ДАО до 4,5—6,5 мкмоль/(л•ч), предшествующий за 14—96 ч гибели больных.
4.Ход практического занятия
1)программированный контроль исходного уровня знаний студентами темы занятия путем устного опроса их по вопросам для самоподготовки;
2)разбор с преподавателем сложных вопросов темы, недостаточно усвоенных студентами при самоподготовке;
3)изучение историй болезни пациентов, имеющих клинические признаки эндогенной интоксикации, проверка умения студентами самостоятельно оценивать результаты анализов и спектрограмм, позволяющих определить стадию и степень тяжести эндогенной интоксикации, разбор клиниколабораторных задач, изученных в процессе самоподготовки;
4)изучение организации работы биохимической лаборатории
многопрофильной больницы, разбор мероприятий по проведению лабораторных тестов на выявление окислительного стресса и эндогенной интоксикации у больных с критическими состояниями и хронической патологией;
5)заключительный контроль знаний студентов (студент при собеседовании с преподавателем должен понимать цель биохимических исследований при эндотоксикозе, решать задания для заключительного тестового контроля).
5.Клинико-лабораторные задачи
ЗАДАЧА 2.1
Больной М., 26 лет, поступил в ожоговое отделение на 4-й день после ожога пламенем II—III Б степени 40% поверхности тела, из них 35% глубоких ожогов. Ожог верхних дыхательных путей I степени. Состояние больного тяжелое. Температура 37,8°С, озноб, тахикардия до 120 уд/мин, АД — 140/90 мм рт. ст. Больной не вступает в контакт, бредит. Отмечается выраженная мышечная дрожь и парез кишечника.
18
Инфузионная терапия и стимулированный диурез эффекта не дают. С целью дезинтоксикационной терапии больному проведена операция плазмафереза с возмещением 1,5 л свежезамороженной плазмы крови.
Лабораторные данные до операции. Эритроциты 3,2 х1012/л, Нв — 120 г/л, лейкоциты — 10,4 х109/л, СОЭ — 28 мм/ч.
Данные биохимических исследований: глюкоза крови 7,2 ммоль/л, мочевина — 5,2 ммоль/л, креатинин — 70 мкмоль/л, общий белок сыворотки крови — 48 г/л, МСиНМэр — 0,9 ед. экст., МСиНМпл — 0,6 ед. экст., МАО — 6,8 мкмоль/(л-ч), ДАО — 3,8 мкмоль/(л-ч). Коэффициент МАО/ДАО = 1,7.
Через сутки после операции плазмафереза лабораторные данные: эритроциты — 3,4х1012/л, Нв = 118 г/л, лейкоциты – 10,6 х109/л, СОЭ — 14
мм/ч.
Данные биохимических исследований: глюкоза крови - 6,8 ммоль/л, мочевина — 5,0 ммоль/л, креатинин — 60 мкмоль/л, общий белок сыворотки крови — 56 г/л, МСиНМэр — 0,7 ед. экст., МСиНМпл — 0,15 ед. экст., МАО — 9,4 мкмоль/(л-ч), ДАО — 2,6 мкмоль/(л-ч). Коэффициент МАО/ДАО = 3,6.
Соответствует ли состояние больного указанным лабораторным данным? Как можно по ним оценить эффективность проведенного плазмафереза? Следует ли планировать повторную операцию плазмафереза?
Что в качестве критерия (помимо состояния больного) следует взять для принятия решения?
Задача 2.2 У больного с почечной недостаточностью в ходе обследования в
биохимической лаборатории установлено, что содержание МСиНМэр составляет 1,3 е.о.п., МСиНМпл составляет 0,9 е.о.п. После курса гемодиализа МСиНМэр составили 1,1 е.о.п., МСиНМпл составляет 0,4 е.о.п.
Вопрос. Какой первичный механизм развития и какая биохимическая фаза эндогенной интоксикации эндогенной интоксикации наблюдается у данного пациента. Какие дополнительные методы биохимического исследования необходимо провести для оценки уровня эндогенной интоксикации. Какая биохимическая фаза эндогенной интоксикации эндогенной интоксикации наблюдается после курса гемодиализа, оцените его эффективность?
Задача 2.3 Трем пациентам выполнено исследование уровней креатинина и
мочевины:
у1-го пациента - уровень креатинина 263 мкмоль/л, уровень мочевины 12 ммоль/л,
у2-го пациента - уровень креатинина 327 мкмоль/л, уровень мочевины 3,1 ммоль/л,
у3-го пациента - уровень креатинина 94 мкмоль/л, уровень мочевины 2,3 ммоль/л.
Вопрос. Определите возможные причины развития описанных патобиохимических состояний.
19
Задача 2.4 У больного с патологией зубов развился абсцесс челюстно-лицевой
области. В ходе обследования в биохимической лаборатории установлено, что содержание МСиНМэр составляет 0,5 е.о.п., МСиНМпл составляет 1,2 е.о.п. Содержание эритроцитов 3,1 Т/л, Нb – 80 г/л.
Вопрос. В период какой биохимической фазы эндогенной интоксикации обратился пациент к стоматологу. Какие дополнительные методы биохимического исследования необходимо провести для оценки уровня эндогенной интоксикации. Какой первичный механизм развития эндогенной интоксикации наблюдается у данного пациента.
Задача 2.5 Двум пациенткам выполнено исследование СОЭ:
у1-й пациентки - показатель СОЭ составил 48 мм/ч (заключение акушерагинеколога: патологических изменений нет),
у2-й пациентки - показатель СОЭ составил 47 мм/ч (заключение акушерагинеколога: установлена наличие беременности).
Вопрос. Определите возможные причины развития описанных состояний и тактику ведения обследованных.
20
