
Министерство образования Республики Беларусь
Учреждение образования
«Белорусский государственный университет
информатики и радиоэлектроники»
Контрольная работа
по дисциплине «Проектирование и производство изделий интегральной электроники»
Выполнил:
Студент 5-го курса заочного отделения группы 990241
Гусев Станислав Павлович
Минск, БГУИР 2023
Содержание
1. Технология термического окисления кремния.
2. Маршрутный процесс формирования диффузионно-планарной структуры:

Технология термического окисления кремния
В течение всего цикла изготовления интегральных схем (ИС) необходимо применение физико-химического процесса, называемого окислением кремния. Двуокись кремния, полученную в ходе данного процесса, используют для формирования межкомпонентной изоляции в ИС, подзатворного диэлектрика в микросхемах, содержащих МОП-структуры, а также в качестве маски при загонке легирующей примеси в необходимые места кремниевой пластины.
Другими словами, функции пленки диоксида кремния (SiO2) можно описать так:
защита, в частности, пассивации участков pn-переходов, выходящих на поверхность;
маска, через которую при локальном легировании (диффузионном или ионном) вводятся необходимые примеси;
тонкий диэлектрик под затвором МОП-транзистора;
диэлектрик межуровневой изоляции систем металлизации.
В технологии ИС различают два вида окислов SiO2 – «толстые» и «тонкие». Толстые окислы обычно имеют d = 0.7-0.8 мкм и выполняют функции защиты и маскировки, а тонкие, имеющие d = 0.1-0.2 мкм, – функции подзатворного диэлектрика в МОП-транзисторах.
При выращивании пленки SiO2 одной из важных проблем является обеспечение ее однородности. В зависимости от качества поверхности пластины, чистоты реагентов и режима выращивания в пленке могут возникать те или иные дефекты. Самый распространенный тип дефектов – микро- и макропоры (в тонком окисле, в частности, вплоть до сквозных отверстий). Кремниевая поверхность всегда покрыта «собственной» окисной пленкой, которая возникает при комнатной температуре в результате «естественного» окисления. Из-за малой толщины пленки, составляющей около 5 нм, невозможно выполнять какую-либо из перечисленных функций. Поэтому технология ИС предполагает получение пленки Si02 искусственным путем.
Термическое окисление кремния проводится в кварцевом или карбид-кремниевом реакторе (трубе) при температурах в диапазоне 700–1200о С в потоке «сухого» кислорода или паров воды. В качестве газов-разбавителей в процессе используются азот или аргон, а для устранения нежелательных загрязнений (примесей) в растущей пленке двуокиси кремния в ходе процесса в реактор может подаваться небольшое количество хлористого водорода (HCl).
Химические реакции, описывающие процесс окисления, имеют следующий вид:
Siтв + О2 SiO2 – при взаимодействии с сухим кислородом;
Siтв + 2H2O SiO2тв + 2H2 – при взаимодействии с влажным кислородом и парами воды.

Рис. 1 – Вид границы раздела монокристаллический кремний – аморфный диоксид кремния
Природа второй реакции более сложна и многоступенчата, и ее нужно именно так и рассматривать.
На первом этапе пары воды вступают в реакцию с ионами кислорода, связывающими кислородно-кремниевые тетраэдры в уже образовавшейся SiO2. H2O+(Si-O-Si) (Si-OH) + (OH-Si).
Далее гидроксильные группы, попадая на границу раздела SiO2 – Si, вступают в реакцию с кремнием. В результате этой реакции образуются окисел и кислород.
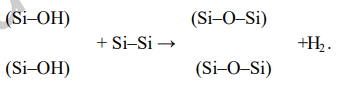
Рис. 2 – Результат химической реакции на границе раздела SiO2 – Si
В дальнейшем водород в растущем оксиде может вступать в реакцию с ионами кислорода, и в результате реакции снова будут образовываться гидроксильные группы.
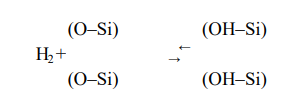
Рис. 3 – Появление гидроксильных групп после реакции с водородом
Такая многоступенчатая реакция способствует увеличению скорости окисления.
Процесс окисления представляет собой диффузионной перенос кислорода через выращенный аморфный слой оксида. (Как уже упоминалось, на поверхности кремния даже при комнатной температуре всегда находится слой естественного оксида, имеющего толщину 3-6 нм). Далее следует его реакция с кремнием на границе Si – SiO2.
Стоит заметить, что при термическом окислении на границе раздела сред образуется переходный слой, который обусловлен перераспределением кислорода. В исходной структуре на поверхности кремния присутствует хемосорбционный слой оксида, состав которого может быть выражен как SiO2-x.
(Хемосорбция – поглощение вещества из паровой фазы или раствора поверхностью твердого тела, при котором между адсорбированными молекулами и поверхностными слоями твердого тела возникает химическое взаимодействие).
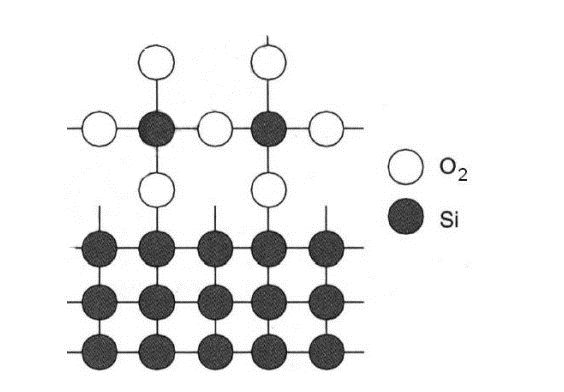
Рис. 4 – Структура границы раздела кремний – диоксид кремния
Концентрация кислорода в этом слое падает от SiO2-x на поверхности Si до нуля на глубине. При окислении за счет протекания диффузно-химических процессов переходный слой формируется не на исходной поверхности подложки, а под ней. При этом сама граница раздела продвигается в объем кристалла. Как следствие, при процессе термического окисления граничный переходный слой формируется в более «чистых» «стерильных» условиях – во внутренних областях кристалла.
Как говорилось ранее, слой двуокиси кремния формируется обычно на кремниевой пластине за счет химического взаимодействия в приповерхностной области полупроводника атомов кремния и кислорода. Кислород содержится в окислительной среде, с которой контактирует поверхность кремниевой подложки, нагретой в печи в диапазоне температур T = 700 – 1200°С. Окислительной средой может быть сухой или влажный кислород. Схематично вид установки показан на рис. 5 (в современных установках пластины в подложкодержателе располагаются вертикально).
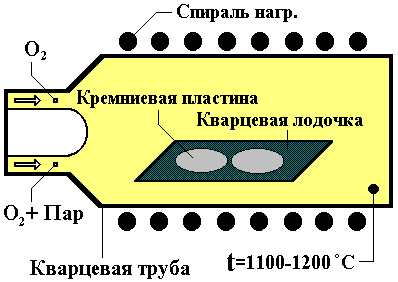
Рис. 5 – Схема установки для окисления
Любая операция, выполняемая на том или ином предприятии, имеет свои допуски и требования к оборудованию. В нашем случае требования коборудованию следующие:
контроль температуры подложкодержателя с точностью до 1 градуса;
обеспечение в реакторе плавного повышения и понижения температуры (двухстадийный нагрев);
отсутствие в реакторе посторонних частиц (подложкодержатель сначала вводится в трубу реактора, а затем опускается на его дно);
отсутствие посторонних примесей, в частности, ионов натрия на внутренней поверхности реактора (чтобы их удалить, труба реактора предварительно продувается хлором);
введение кремниевых пластин в реактор сразу после их химической очистки.
Уравнения химических реакций, происходящих на поверхности кремниевой пластины, описаны выше, но к ним можно добавить еще две химические реакции: термическое окисление в присутствии хлора (хлорное окисление) и пирогенное окисление – термическое окисление при взаимодействии молекул воды, синтезированных из атомарно чистых кислорода и водорода непосредственно у поверхности кремния, с атомами кремния.
Время окисления в стандартных технологических процессах находится в диапазоне 4-5 часов, а если сравнивать сухое окисление с влажным, то сухое идет в разы медленнее. Например, для выращивания пленки SiO2 толщиной 0,5 мкм в сухом кислороде при 1000 °С требуется около 5 ч, а во влажном – всего 20 мин. С уменьшением температуры на каждые 100 °С время окисления возрастает в 2-3 раза.
Значительным достижением в совершенствовании технологии окисления кремния явилось добавление в окислительную среду в процессе окисления хлорсодержащих компонентов. Это привело к улучшению стабильности порогового напряжения полевых МДП транзисторов, увеличению напряжения пробоя диэлектриков и повышению скорости окисления кремния. Главная роль хлора в пленках двуокиси кремния (обычно с концентрацией хлора 1016 – 1020 см-3) заключается в превращении случайно проникших в SiO2 примесных ионов натрия или калия в электрически неактивные.
Основными контролируемыми параметрами пленок являются: коэффициент преломления, химический состав пленки, пористость, плотность, скорость травления, напряженность поля пробоя. Значения некоторых типичных характеристик термических пленок SiO2 таковы:
Плотность, г/см3 – 2.2;
Показатель преломления – 1.47;
Диэлектрическая постоянная – 3.82;
Ширина запрещенной зоны, эВ – 8.9;
Удельное сопротивление постоянному току при T = 25 °С, Ом·см – 1014-1016;
Скорость травления в буферном растворе HF, нм/мин – 100;
Линия ИК поглощения, мкм – 9.3;
Коэффициент теплового расширения, С-1 – 5·10-7;
Механические напряжения в окисле, дин/см2 – 3·109.
