
805
.pdf
Лабораторная работа № 10 Определение теплоты сгорания топлив
Тема: «Топлива энергетических установок».
Цель:
-ознакомиться с промышленным методом определения теплоты сгорания топлив;
-выявить влияние соотношения компонентов топлива на теплоту сгорания на примере углеводородного горючего и воздуха как окислителя.
Содержание работы
Объектом исследования является навеска бензина в ампуле, находящейся в герметичном сосуде (калориметрической бомбе) в среде окислителя (воздуха); предметом – выявление влияния коэффициента избытка окислителя на теплоту сгорания топлива.
Последовательность проведения эксперимента:
-определить навеску бензина в ампуле;
-вычислить стехиометрическое соотношение компонентов бензина и воздуха;
-рассчитать потребное давление наполнения калориметрической
бомбы воздухом для заданного значения ; - подготовить установку к работе и провести эксперимент по опре-
делению теплоты сгорания бензина в воздухе при заданном ; - на основании опытов представить графическую зависимость
Hв=f(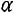 );
);
- сделать выводы по результатам работы.
Краткие сведения из теории Под теплотой сгорания топлива понимают тепловой эффект ре-
акции горения, отнесенный к 1 кг топлива. Если продукты реакции охлаждены до начальной температуры и водяные пары находятся в сконденсированном состоянии, то теплота сгорания называется высшей и обозначается HB. Если пары воды не сконденсированы, то такая теплота сгорания называется низшейз (НН). Условия проведения эксперимента на установке дают возможность определить HВ.
Отношение массы окислителя к массе горючего при сгорании топлива называют действительным соотношением компонентов.
Его обозначают К и вычисляют по формуле:
71

K |
mок |
, |
кгок |
. |
|
|
|||
|
mгор |
|
кггор |
|
Для полного сгорания одного килограмма горючего требуется вполне определенное количество окислителя. В этом случае соотношение компонентов именуют стехиометрическим. Обозначают стехиометрическое соотношение через Ко и вычисляют по формуле:
|
|
|
ibi |
гор |
|
кг |
|
|
К |
|
|
|
, |
ок |
, |
|
о |
|
|
||||
|
|
|
|
кггор |
|||
|
|
|
ibi |
ок |
|
||
где |
– валентность i-го элемента; |
|
|
|
|
||
|
– число грамм-атомов i-го элемента в условной химической |
||||||
формуле компонента. |
|
|
|
|
|
|
|
|
Отличие действительного от стехиометрического соотношения |
||||||
устанавливается коэффициентом избытка окислителя : |
|||||||
|
|
|
= К / Ко. |
|
|
||
|
Очевидно, что максимальное значение теплоты сгорания топ- |
||||||
лива должно соответствовать значению |
|
= 1. |
|
||||
Устройство и принцип работы лабораторной установки
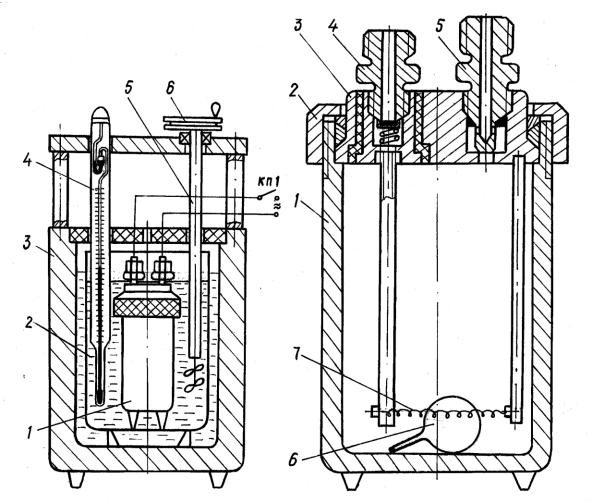
Для экспериментального определения теплоты сгорания топлива Hв используется калориметрическая установка промышленного типа. Еѐ схема показана на рис. 2.16. Основным элементом установки является калориметрическая бомба 1, в которой происходит сгорание топлива. Бомба помещается в калориметрический сосуд 2, предварительно заполненный определенным количеством воды.
Подъем температуры воды при сгорании топлива замеряется метастатическим термометром 4. Выравнивание поля температуры в сосуде осуществляется путем перемещения воды мешалкой 5, приводимой в движение маховиком 6.
Калориметрический сосуд устанавливается в двустенный кожух калориметра 3. Внутреннее межстенное пространство кожуха заполняется водой с целью уменьшения теплообмена калориметрического сосуда с внешней средой.
Метастатический термометр относится к числу стеклянных ртутных термометров со вложенной шкальной пластиной и имеет рабочую шкалу 5 оС с ценой деления 0,01 оС и вспомогательную шкалу от –20 до +150 оС с ценой деления 5 оС. На вспомогательной шкале устанавливают нижний предел температуры, от которого
72
производят отсчет по рабочей шкале путем переливания части ртути из капилляра в сифонообразный вспомогательный резервуар. Основная допустимая погрешность термометра 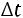 = 0,015 оС. Температуру измеряют, погрузив термометр в измеряемую среду на постоянную величину до начала делений шкалы.
= 0,015 оС. Температуру измеряют, погрузив термометр в измеряемую среду на постоянную величину до начала делений шкалы.
Калориметрическая бомба (см. рис. 2.17) состоит из толстостенного цилиндрического стакана 1, крышки бомбы 3 с накидной гайкой 2. В крышку ввернуты два штуцера. Штуцер 4 служит для наполнения бомбы газообразным окислителем, штуцер 5 является выпускным клапаном. Кроме того, через штуцера подается напря-
Рис. 2.16 |
Рис. 2.17 |
жение для организации воспламенения топлива. С целью зажигания навески горючего токовводы перемыкаются нихромовой проволочкой 7 диаметром 0,2 мм. При нажатии кнопки КП1, электрический ток напряжением не более 6В поступает на проволочку и надежно воспламеняет топливо. Теплота, выделившаяся при сгорании топлива, идет на нагрев калориметрической системы, включающей бомбу и калориметрический стакан с водой и мешалкой. Если известен во-
73
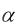
дяной эквивалент этой системы W, равный произведению массы системы на условную ее теплоемкость, то по подъему температуры воды после воспламенения можно судить о количестве теплоты сгорания топлива.
Исходные данные
В эксперименте в качестве горючего используется бензин с условной химической формулой С72,25 Н133; в качестве окислителя – воздух, условная химическая формула которого N75,5 O14,5. Внутренний объем калориметрической бомбы V= 0,25 л.
Экспериментальная часть работы
Основные этапы работы:
-проверка исходного состояния установки;
-подготовка к эксперименту;
-проведение эксперимента;
-приведение установки в исходное состояние.
Все операции выполняются согласно документации на установку под руководством преподавателя.
Проверка исходного состояния подразумевает проверку наличия воды в сосуде 2, чистоту бомбы 1, целостности контактных проводов, надежности крепления нихромовой проволочки к токовводам.
Подготовка к эксперименту состоит в выполнении следующих операций:
-заполнение колбы горючим (бензином А-80);
-определение массы горючего в колбе;
-определение стехиометрического соотношения компонентов топлива.
При заданном 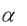 вычисляется потребная масса окислителя:
вычисляется потребная масса окислителя:
mок = mгор Ko ;
По массе окислителя определяется величина абсолютного давления наполнения бомбы воздухом:
p =mок RT/ V,
где R – газовая постоянная воздуха, Дж/кг • К;
Т – температура воздуха при наполнении бомбы, К; V – объем бомбы, м3.
Последовательность проведения эксперимента:
-установить крышку бомбы 3 (рис. 2.17) на специальный штатив;
-разместить на дне бомбы 1 колбочку 6 с горючим;
74
-вставить крышку в стакан до упора;
-завернуть накидную гайку 2;
-перенести бомбу в вертикальном положении на стол для наполнения воздухом;
-наполнить бомбу воздухом, для чего:
-навернуть трубку от воздушного редуктора на впускной штуцер;
-нагрузить редуктор, доведя давление в бомбе до расчетного;
-встряхнуть бомбу, с целью механического разрушения ампулы с бензином;
-установить бомбу в сосуд;
-подсоединить контактные провода;
-установить мешалку и термометр;
-закрыть кожух крышкой;
-включить в работу мешалку (она не должна касаться стенок сосуда и бомбы и выходить из воды);
-через 5 - 7 мин (это время необходимо для выравнивания температуры всех частей калориметрической системы) сделать первый отсчет показания термометра;
-замкнуть ток в цепи зажигания;
-следить за подъемом температуры по термометру;
-зафиксировать максимальное значение температуры;
-снять с установки напряжение;
-разобрать калориметрическую систему;
-стравить из бомбы продукты сгорания;
-разобрать бомбу;
-промыть и просушить бомбу.
Расчетная часть работы
Задача расчета состоит в определении величины теплоты сгорания как функции от коэффициента избытка окислителя.
Предлагается следующая последовательность расчета:
- вычислить высшую теплоту сгорания топлива при заданном коэффициенте избытка окислителя:
Hв = W(t2 – t1)/mт ,
где W – водяной эквивалент калориметрической системы, Дж/К (обозначен на установке);
t1 и t2 – начальная и конечная температура воды в калориметрическом сосуде, 0C;
mт – масса топлива, кг;
75

-сравнить величину высшей теплоты сгорания Hb с величинами, полученными на других установках при других значениях избытка окислителя;
-построить зависимость Hb = f(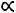 );
);
-сделать выводы по работе.
Содержание отчета
Кроме оформленного заголовка отчет должен содержать:
1.Схему лабораторной установки.
2.Сведения об измерительных приборах.
3.Расчетные формулы.
4.Исходные данные.
5.Результаты измерений и вычислений.
6.Выводы.
Выводы по данной работе должны содержать объяснение зависимости Нb = f( ) и оценку точности полученного значения Hb при
= 1 в сравнении с табличным.
Контрольные вопросы по теме лабораторной работы
1.Перечислите назначение и состав лабораторной установки.
2.Перечислите порядок обработки экспериментальных данных.
3.Поясните, что понимается под топливом.
4.Поясните, как определяется условная химическая формула компонента топлива.
5.Поясните, что такое стехиометрическое соотношение компонентов топлива.
6.Поясните, что понимают под коэффициентом избытка окислителя.
7.Поясните, что понимают под высшей и низшей теплотой сгорания топлива.
76
Библиографический список
1. Богданов, С.Н. Холодильная техника. Свойства веществ : справочник / С.Н. Богданов, О.П. Иванов, А.В. Купреянов – М.:
Агропромиздат, 1985, – 320 с.
2.Захаров, А.А. Практикум по применению теплоты и теплоснабжению в сельском хозяйстве. – М.: Колос, 1995. – 176 с.
3.Кошман, В.С. Словарь терминов и определений по гидравлике, теплотехнике и газовой динамике / В.С. Кошман, А.Т. Манташов.
–Пермь: ФГБОУ ВПО Пермская ГСХА, 2013. – 56 с.
4.Манташов, А.Т. Теплофизика: руководство для лабораторных занятий / А.Т. Манташов, С.И. Рожков – Пермь: МО РФ, 2000 – 71 с.
5.Манташов, А.Т. Теплотехника. ч. I. Термодинамика и теплопередача / А.Т. Манташов. – Пермь: ПГСХА, 2009. – 184 с.
6.Манташов, А.Т. Теплотехника ч. II. Теплотехническое обеспечение обитаемости объектов сельскохозяйственного назначения: учебное пособие. – Пермь: ФГБОУ ВПО «Пермская ГСХА, 2011. –
118 с.
7.Преображенский, В.П. Теплотехнические измерения и при-
боры. – М.: Энергия, 1978 – 704 с.
8.Теплоэнергетика и теплотехника: справочник / под общей ред. В.А. Григорьева, В.М. Зорина. – М.: Энергия, 1980. – 530 с.
77

Приложение
Т а б л и ц а 1
78
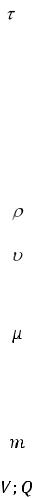
Т а б л и ц а 2
Обозначения и единицы измерения физических величин
|
|
|
|
Обозна- |
|
|
Обо- |
Наименование |
чение |
Наименование |
|
едини- |
||
|
значе- |
единицы измерения |
||
|
|
цы |
||
|
|
ние |
|
|
|
|
|
измере- |
|
|
|
|
|
|
|
|
|
|
ния |
|
Основные единицы |
|
||
Длина |
|
|
метр |
м |
|
|
|
|
|
Масса |
|
m |
килограмм |
кг |
Время |
|
; t |
секунда |
с |
Термодинамическая тем- |
|
T |
кельвин |
К |
пература |
|
|||
|
|
|
|
|
Температура Цельсия |
|
t |
градус Цельсия |
0С |
Количество вещества |
|
М |
моль |
моль |
|
|
|
|
|
Производные единицы |
|
|||
Площадь |
|
F; S |
квадратный метр |
м2 |
Объем |
|
V |
кубический метр |
м3 |
Плотность |
|
|
килограмм на кубиче- |
кг/м3 |
|
|
|
ский метр |
|
Удельный объем |
|
|
кубический метр на |
м3/кг |
|
|
|
килограмм |
|
Удельный вес |
|
γ |
ньютон на кубический |
Н/м3 |
|
|
|
метр |
|
Молярная масса |
|
|
килограмм на моль |
кг/моль |
|
|
|
|
|
Давление |
|
р |
паскаль |
Па |
|
|
|
|
|
Скорость |
|
c |
метр в секунду |
м/с |
Скорость звука |
|
a |
метр в секунду |
м/с |
Массовый расход, массо- |
|
|
килограмм в секунду |
кг/с |
вая подача |
|
|
||
|
|
|
|
|
Объемная подача. Объем- |
|
|
кубический метр в се- |
м3/с |
ный расход |
|
|
кунду |
|
Вес |
|
G |
ньютон |
Н |
|
|
|
|
|
Сила |
|
P |
ньютон |
Н |
|
|
|
|
|
Энергия |
|
E |
джоуль |
Дж |
|
|
|
|
|
Мощность |
|
N |
ватт |
Вт |
|
|
|
|
|
Количество теплоты |
|
Q |
джоуль |
Дж |
|
|
|
|
|
Приведенная теплота |
|
q |
джоуль на килограмм |
Дж/кг |
|
|
|
|
|
Работа |
|
L |
джоуль |
Дж |
|
|
|
|
|
|
79 |
|
|
|

Приведенная работа |
|
l |
джоуль на килограмм |
Дж/кг |
|
|
|
|
|
|
|
Внутренняя энергия |
U |
джоуль |
Дж |
||
|
|||||
|
|
|
|
|
|
Приведенная внутренняя |
|
u |
джоуль на килограмм |
Дж/кг |
|
энергия |
|
||||
|
|
|
|
|
|
Энтальпия |
I; H |
джоуль |
Дж |
||
Удельная энтальпия |
i; h |
джоуль на килограмм |
Дж/кг |
||
|
|
|
|
|
|
Энтропия |
|
S |
джоуль на кельвин |
Дж/К |
|
Удельная энтропия |
|
s |
джоуль на килограмм - |
Дж/(кг∙ |
|
|
кельвин |
К) |
|||
|
|
|
|
||
Теплота фазового перехо- |
|
r |
джоуль на килограмм |
Дж/кг |
|
да |
|
||||
|
|
|
|
|
|
Газовая постоянная |
|
R |
джоуль на килограмм- |
Дж/(кг∙ |
|
|
кельвин |
К) |
|||
|
|
|
|
||
Универсальная газовая по- |
|
|
|
джоуль на молькель- |
Дж/(мол |
стоянная |
|
|
|
вин |
ь К) |
Ускорение свободного |
|
g |
метр на секунду в |
м/с2 |
|
падения |
|
|
|
квадрате |
|
Коэффициент температур- |
|
|
|
паскаль в минус пер- |
Па -1 |
ного расширения |
|
|
|
вой степени |
|
Динамический коэффици- |
|
|
|
паскаль - секунда |
Па |
ент вязкости |
|
|
|
||
|
|
|
|
|
|
Кинематический коэффи- |
|
|
|
квадратный метр в се- |
м2/с |
циент вязкости |
|
|
|
кунду |
|
Теплоемкость удельная |
|
c |
джоуль на килограмм- |
Дж/(кг∙ |
|
массовая |
|
кельвин |
К) |
||
|
|
|
|||
Теплоемкость удельная |
|
|
|
джоуль на моль- |
Дж/( |
молярная |
|
|
|
кельвин |
моль |
с |
|||||
|
|
|
|
|
К) |
Теплоемкость удельная |
|
|
|
джоуль на кубиче- |
Дж/( |
объемная |
|
|
|
ский метр - кельвин |
м3 К) |
Теплоемкость удельная |
|
|
|
джоуль на кило- |
Дж/(к |
при постоянном давле- |
|
|
|
||
|
|
|
граммкельвин |
г∙К) |
|
нии |
|
|
|
||
|
|
|
|
|
|
Теплоемкость удельная |
|
|
|
джоуль на кило- |
Дж/(к |
при постоянном объеме |
|
|
|
грамм - кельвин |
г∙К) |
Тепловой поток |
|
|
|
ватт |
Вт |
|
|
|
|
|
|
Плотность теплового по- |
|
|
|
ватт на квадратный |
Вт/м2 |
тока |
|
|
|
метр |
|
Температурный градиент |
grad T |
кельвин на метр |
К/м |
||
|
|
|
|
|
|
Коэффициент теплопро- |
|
|
|
ватт на метр - кельвин |
Вт/(м∙К) |
водности |
|
|
|
||
|
|
|
|
|
|
|
80 |
|
|
||
