- •Глава 2. Молекулярные Механизмы взаимодействия озона c компонентами живых клеток
- •2.1.Озонолиз
- •2.2. Реакции озона с индивидуальными компонентами
- •2.2.1. Реакции озона с липидами.Перекисное окисление липидов
- •2.2.2. Реакции озона с аминокислотами и белками
- •2.2.3. Реакции озона с аминами
- •2.2.4. Взаимодействие озона с нуклеиновыми кислотами
- •2.2.5. Реакции озона с надн и надфн
- •2.2.6. Реакции озона с регуляторами роста и развития
- •2.3.1.Cвободные радикалы
- •2.3.2.Перекиси
- •2.3.3. Механизмы действия активных форм кислорода, образуемых озоном
2.2.2. Реакции озона с аминокислотами и белками
Окислительным превращениям при действии озона подвергаются практически все аминокислоты, но особенно триптофан, тирозин, гистидин, цистеин, хотя и в разной степени. Эта реакция более характерна для цистеина и цистина, и в меньшей – для тирозина, фенилаланина, триптофана. Высокая реакционная способность серусодержащих аминокислот обусловлена сравнительно легкой поляризуемостью сульфгидрильных SH и сульфуглеродных SC- групп, которые служат местом атаки электронов. Под влиянием озона возможно образование различных продуктов в следующих реакциях :
цистеин (RSH) цистин (RSSR),
цистеин (RSH) цистеиновая кислота (RSO3H),
метионин (CH3SR) метионинсульфоксид (CH3SOR),
триптофан (С11H12N2O2) N-формилкинугенин
Озон вызывает деструкцию белковых молекул. Специфика их окислительной модификации определяется особенностью аминокислотного состава и структурной организацией белковых молекул. Предполагается, что с озоном реагируют аминокислотные остатки белков. Он также окисляет белковые тиолы с образованием дисульфидных мостиков между белковыми цепочками. За счет способности реагировать с тиоловыми группами цистеина наибольшей чувствительностью к озону, обладает, например, белок млечного сока дынного дерева - папаин. Белки лиизоцим и овидин чувствительны к озону за счет окисления их аминокислотных остатков, главным образом, триптофана.
2.2.3. Реакции озона с аминами
Реакции озона с аминами протекают довольно легко. Механизм реакции для аминов зависит от строения исходного амина. По современным представлениям, амин R3N реагирует с озоном в реакции:
R3N + O3 R3 N+OOO
В результате образуется озонид, который затем разлагается, теряя молекулярный кислород
R3 N+ OOO- R3N+ O + O2
Катехоламины дофамин, норадреналин, адреналин реагируют с озоном как обычные фенолы, присоединяясь по двойным связям, далее их окисление идет до красных пигментов аминохромов, а затем и - черных пигментов меланинов.
2.2.4. Взаимодействие озона с нуклеиновыми кислотами
Озон реагирует с двойными связями азотистых оснований нуклеиновых кислот, образуя озониды, в конечном итоге происходит образование разрывов в одиночных или двойных спиралях. Эти повреждения вызывают снижение нормальной генетической функции ДНК. Как установлено в работах на животных, растениях, микроорганизмах и клеточных культурах, озон является мутагеном. Мутации возникают даже при коротких экспозициях при концентрации 0,1 до 1,0 частей на млн. С увеличением концентрации и продолжительности экспозиции частота мутаций увеличивается. Мутагенные свойства озона связаны с его способностью вызывать дефекты в структурах нуклеиновых кислот. Кроме того, озон нарушает включение азотистых оснований в структуру ДНК при ее синтезе.
2.2.5. Реакции озона с надн и надфн
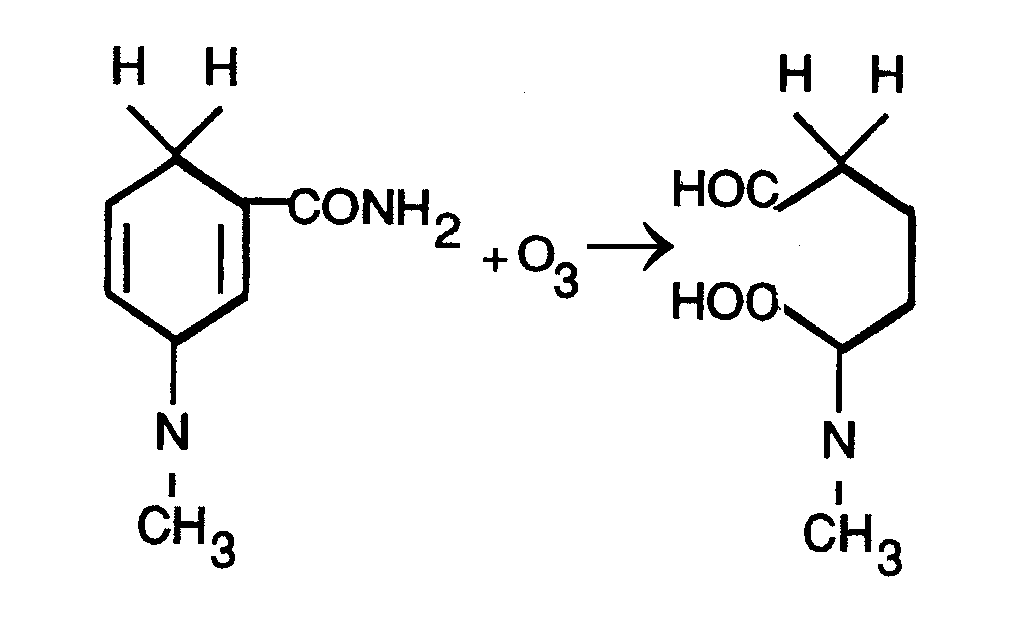
Биологически важные восстановители, такие как никотинамидадениннуклеотид (НАД) и никотинамидадениндинуклео-тидфосфат (НАДФ) в восстановленной форме легко окисляются озоном (рис. 12).
|
Рис.12. Реакция озона с НАДН |
При действии озона происходит разрыв ароматического кольца с образованием альдегидных групп в месте разрыва. Озонолиз вначале идет по 5-6 двойной связи, а затем по 2-3 двойной связи. Реакция зависит от рН и протекает с большой скоростью в нейтральной и щелочной средах. НАД и НАДФ более устойчивы к озону, чем их восстановленные формы. Следует отметить, что продукты реакции НАДН и НАДФН с озоном не обладают биологической активностью.