
- •1.Общие понятия о лигнине. Особенности строения лигнина лиственных и хвойных пород.
- •3. Технические лигнины: виды, свойства, применение.
- •4. Физические свойства лигнина. Доказательства ароматического строения лигнина.
- •5. Метоксильные группы лигнина: содержание и способы определения .
- •6. Гидроксильные группы лигнина: виды, содержание и способы определения.
- •7. Карбонильные и карбоксильные группы лигнина: содержание и способы определения .
- •8. Этиленовые двойные связи в лигнине: содержание и способы определения
- •9. Основные типы связей в лигнине. Основные димерные структурные единицы лигнина.
- •10. Основные связи лигнина с углеводами.
- •11.Особенности химических реакций лигнина
- •12. Взаимодействие лигнина с хлором
- •13. Взаимодействие лигнина с азотной кислотой
- •14. Окисление лигнина
- •15. Гидрогенолиз лигнина
- •16. Взаимодействие лигнина с нуклеофильными реагентами в кислой среде
- •17. Взаимодействие лигнина с нуклеофильными реагентами в щелочной среде
- •18. Реакции элиминирования лигнина
- •19. Реакции конденсации лигнина
5. Метоксильные группы лигнина: содержание и способы определения .
Лигнин – полифункциональный полимер включающий: 1) метоксильные группы; 2) гидроксильные (фенольные и алифатические); 3) карбонильные (альдегидные и кетонные); 4)карбоксильные; 5) двойные связи алкенового типа.
Метоксильные группы (-ОСН3)Содержание: 1) лигнин хвойных пород 15-17%; 2) лигнин лиственных пород 20-22%. Содержание Ме – критерий оценки качества препарата лигнина.
Определение содержания Ме: Метод Цейзеля – расщепление простых эфиров концентрированной кислотой НI:
Ar–OCH3 + HI → Ar–OH + CH3I.
Летучий иодистый метил определяют: 1) Гравиметрическим методом (весовым); 2) Титриметрическим методом; 3) Хроматографическим методом.
6. Гидроксильные группы лигнина: виды, содержание и способы определения.
Гидроксильные группы. В лигнине присутствуют фенольные (в ароматическом кольце) и алифатичские (спиртовые, в пропановой цепочке) гидроксильные группы (первичные и вторичные). Также они могут быть свободными и связанными

Структурные единицы со свободными фенольными гидроксилами называют фенольными.
Структурные единицы со связанными фенольными гидроксилами – нефенольные единицы.
Общее содержание свободных ОН-групп:
- 1,1-1,2 на ФПЕ или
-110-120 групп на 100 ФПЕ
Определение общего содержания ОН-групп:
Способ 1. Исчерпывающее метилирование диметилсульфатом в присутствии щелочи:
R–OH + (CH3)2SO2 + NaOH → R–OCH3 + Na(CH3)SO4 + H2O.
По разности содержания метоксильных групп до и после метилирования определяют содержание гидроксильных групп (определяют по увеличению Ме);
Способ 2. Ацетилирование лигнина уксусным ангидридом в пиридине (пиридин – катализатор):
R–OH + (CH3CO)2O → R–OCOCH3 + CH3COOH.
Количество групп рассчитывают по выделившейся уксусной кислоте. Оттитровывают выделившуюся уксусную кислоту.
Определение содержания фенольных ОН-групп:
В препаратах лигнина массовая доля свободных фенольных гидроксилов составляет 1–3%.
Хвойный лигнин 0,2-0,3 на ФПЕ
Лиственный лигнин 0,1-0,4 на ФПЕ
Методы:
– метилирование диазометаном:
Ar–OH + CH2N2 → Ar–OCH3 + N2↑.
Массовую долю фенольных гидроксильных групп рассчитывают по увеличению содержания метоксильных групп.
– хемосорбционный метод, основанный на ионном обмене между кислыми группами лигнина и раствором гидроксида бария:
2 Ar–OH + Ba(OH)2 → (Ar–O)2Ba + H2O; затем оттитровывают избыток Ba(OH)2
2 R–COOH + Ba(OH)2 → (Ar–O)2Ba + H2O.
- модифицированный барий-хлоридный метод:
Ar–OH + NaOH ↔ Ar–ONa + H2O;
2 Ar–ONa + BaCl2 → 2 Ar–OBa0,5 + 2 NaCl.
Избыток гидроксида натрия оттитровывают. Вследствие нерастворимости бариевых солей (фенолятов) лигнина равновесие первой реакции полностью сдвигается вправо;
Алифатические (спиртовые) гидроксильные группы находятся в пропановых цепях в количестве 0,8–0,9 группы на ФПЕ, т.е. почти каждая фенилпропановая структурная единица лигнина имеет свободный спиртовой гидроксил.
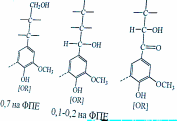
Распределение ОН-групп: 1) первичные спиртовые – 0,7 на одну ФПЕ; 2) вторичные – в α-положении 0,1-0,2 на ФПЕ
В препаратах могут быть группировки кетонов с гидроксилом в β-положении и кетонной группой в α-положении.
Наиболее высокую реакционную способность имеют вторичные гидроксильные группы в α-положении – бензилспиртовые.
Определение спиртовых ОН-групп:
- Первичные: реакция отщепления ϒ-атома при нагревании:
R–CH2OH +28% H2SO4 → R–Н + CH2O.
Расчет ведут по выходу формальдегида.
Спиртовые группы (вторичные) в α-положении легко метилируются при действии мети-лового спирта в присутствии 0,5%-ной соляной кислоты при комнатной темпера-туре:
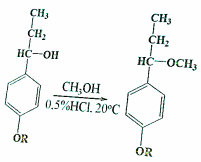
Количество вторичных спиртовых групп определяют по разности меток-сильных групп до и после метилирования.
