
книги / Теория химических реакторов введение в основной курс
..pdf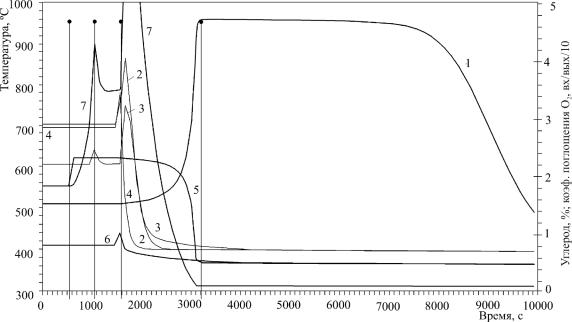
181
Рис. 61. Температура и углерод по слоям катализатора. Углерод в поступающем катализаторе 1,8 %, Тк = 510 °С, циркуляция 30 т/ч, воздух 20 т/ч. Скачок концентрации углерода на 616-й секунде до 2,3 %. Внезапная остановка катализатора на 1554-й секунде: 1 – температура термонапряженного слоя (5 м, T max = 5 °С); 2 – температура на термопаре I (0,087 м); 3 – температура на термопаре II (2,587 м); 4 – температура нижнего слоя 0 м; 5 – углерод термонапряженногослоя; 6 – углероднижнегослоя; 7 – коэффициентпоглощениякислородавверхнейсекции/10
181
182
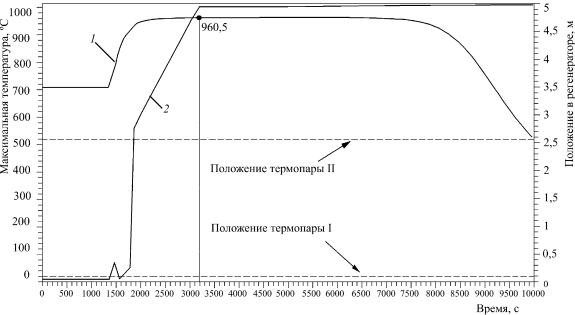
Рис. 62. Максимальная температура. Углерод в поступающем катализаторе 1,8 %, Тк = 510 °С, циркуляция 320 т/ч, воздух20 т/ч. Скачокконцентрацииуглеродана616-йсекундедо2,3 %. Внезапнаяостановкакатализатора на 1554-й секунде: 1 – максимальная температура, °С; 2 – положение термонапряженного слоя, м
182
183
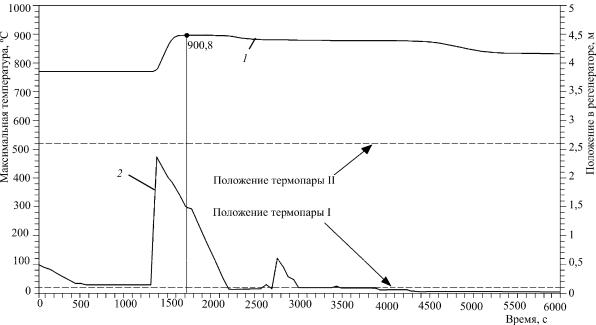
Рис. 63. Максимальная температура. Углерод в поступающем катализаторе 1,8 %, Тк = 510 °С, циркуляция 200 т/ч, воздух 20 т/ч. Скачок концентрации углерода на 613-й секунде до 2,3 %:
1 – максимальная температура, °С; 2 – положение термонапряженного слоя, м
183

Факт появления подобных температурных вспышек зафиксирован при работе промышленной установки каталитического крекинга КК-1 ООО «ЛУКОЙЛ-Пермнефтеоргсинтез». Причиной появления этих вспышек являлась тепловая неустойчивость реактора окисления, описанная в подразд. 11.2.
12.3. Упрощенная модель регенератора
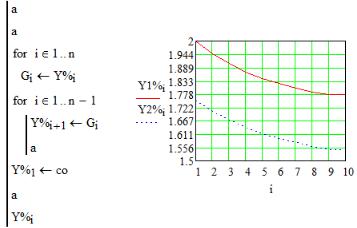
Упрощенная математическая модель в системе Mathcad для варианта противоточного движения газа-окислителя и без учета разогрева катализатора при выжиге кокса имеет следующий вид:
Основные параметры расчета: n – количество интервалов расчета по высоте первой секции регенератора; co – начальное содержание кокса на катализаторе, мас. %; oo – начальное содержание кислорода в окислителе, мас. %; H – высота секции регенера-
184

тора, м; B – расход окислителя , т/ч; Q – расход катализатора, т/ч; tkn – температура катализатора, °С; f – площадь квадратной площадки, выделенная на поверхности катализатора, м2; D – внутренний диаметр реактора (регенератора), м; P – давление в регенераторе, атм.; NKB – количество объемов воздуха, приходящееся на один объем катализатора.
При проведении вычислений в математическую модель введен настроечный коэффициент проскока реагентов по высоте слоя катализатора (подразд. 8.1) за счет введения поправочных коэффициентов при расчете Аi во внутреннем цикле программы, равных 2,8303 и 4,245 соответственно.
Продолжение программы представлено на рис. 64.
Рис. 64. Последовательный процесс выжигания кокса в первой секции (Y1% – содержание углерода в катализаторе, % мас.)
и во второй секции регенератора (Y2 %)
185
13. КИНЕТИЧЕСКАЯ МОДЕЛЬ СТАДИИ СИНТЕЗА ПЕНТАЭРИТРИТА
Пентаэритрит получается конденсацией ацетальдегида и формальдегидавщелочнойсредепоследующимуравнениям:
NaOH |
(248) |
CH3CHO 3HCOH (CH2OH)3 CCHO; |
(CH2OH)3 CCHO HCOH NaOH
(249)
(CH2OH)4 C HCOONa;
CH3CHO 4HCOH NaOH
(250)
(CH2OH)4 C HCOONa.
Реакция представляет собой двухстадийный процесс, включающий альдольную конденсацию трех молекул формальдегида
иодной молекулы ацетальдегида с образованием пентаэритрозы
ипоследующую перекрестную реакцию Канниццаро, идущую между пентаэритрозой и формальдегидом в щелочной среде, в результате которой образуется пентаэритрит и формиат натрия в качестве побочного продукта.
При избытке формальдегида и наличии щелочных реагентов эти реакции идут одновременно и синтез пентаэритрита осуществляется в одну стадию.
Параллельно с основным процессом идет образование дипентаэритрита:
CH3CHO 4HCOH NaOH C(CH2OH)4 |
|
(CH2OH)3 CCH2OCH2C(CH2OH)3 |
(251) |
HCOONa H2O. |
|
Примеси дипентаэритрита снижают качество пентаэритрита. Взаимодействие пентаэритрита и дипентаэритрита с избыточным количеством формальдегида в реакционной смеси приводит к образованию формалей моно- и дипентаэритритов различного строения, малорастворимыхвводе, атакжедругихпобочныхпродуктов.
186
Пентаэритрит образуется при взаимодействии непредельных органических соединений, одним из главных химических свойств которых является способность к полимеризации за счет раскрытия двойных связей. Эта особенность позволяет продолжить реакцию в сторону образования более сложных линейных и циклических соединений, являющихся побочными продуктами синтеза, которые достаточно трудно выделить в чистом виде. Кроме того, эти соединения при высокой себестоимости их выделения не имеют широкого применения, в связи с чем они просто уничтожаются во избежание нанесения экологического ущерба окружающей природной среде. Учитывая, однако, что доля образующихся побочных продуктов достаточно высока, любое усовершенствование процесса, приводящее к снижению выхода побочных соединений, может вызвать интерес производственников.
Механизм процесса исследован неоднократно. Одна из схем протекающих реакций приведена на рис. 65.
Очевидно, что воспользоваться предложенной схемой химических реакций практически невозможно из-за отсутствия значений констант скоростей реакций, протекающих по данной схеме. Упрощение механизма, безусловно, приводит к уменьшению степени адекватности модели, поэтому при ее разработке необходимо выдержать определенный баланс между желаемой точностью описания процесса и погрешностью вычисления концентраций основных продуктов синтеза.
Достаточной точности модели синтеза можно добиться, применяя метод ключевых реакций, аналогичный методу групповых компонентов [11], представленный ниже.
Более простой, формальный, механизм процесса основан на представлении об образовании сложного молекулярного комплекса в ключевой реакции, являющегося носителем основных реакций синтеза:
1 |
CH |
CHO HCOH |
1 |
k1 |
1 |
Complex. |
(252) |
|
|
NaOH |
|
||||
4 |
3 |
|
4 |
k2 |
4 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
187 |
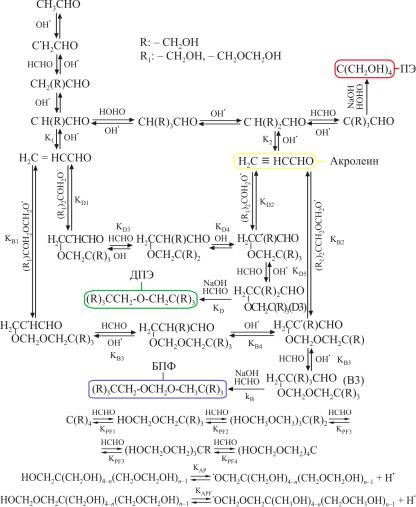
Рис. 65. Кинетическая схема процесса производства пентаэритрита
Далее, процессы внутренних перестроек этого комплекса приводят к образованию пентаэритрита, при взаимодействии его с различными продуктами реакции последовательно получаются остальные органические соединения:
188
|
k3 |
|
OH) |
|
HCOONa, |
(253) |
||
|
Complex C (CH |
4 |
||||||
|
k4 |
2 |
|
|
|
|
|
|
|
Complex C(CH2OH)4 |
k5 |
|
|
||||
|
, |
|
(254) |
|||||
|
|
|
|
|
|
k6 |
|
|
(CH2OH)3 CCH2OCH2C(CH2OH)3 HCOONa H2O, |
|
|||||||
|
|
|
|
|
|
k7 |
|
|
|
1 Complex C(CH2OH)4 2 HCOH , |
|
||||||
|
3 |
|
|
3 |
k8 |
|
(255) |
|
2 |
(CH2OH)3CCH2O |
|
|
1 HCOONa |
2 H2O. |
|||
CH2 + |
|
|||||||
3 |
2 |
|
|
3 |
|
|
3 |
|
|
|
|
|
|
|
|
|
|
Обрыв цепи протекающих реакций установлен искусственно на реакции (255), конечным продуктом которой является биспентаэритрит формаль (БПФ). Поскольку концентрация еще более высокомолекулярных побочных продуктов достаточно мала, такой обрыв цепи реакций не должен внести большой погрешности в результатымоделирования.
На основании закона действующих масс К. Гульдберга и П. Вааге, а также дополнения Н.И. Бекетова, дальнейшим этапом работы является составление математической модели и системы дифференциальных уравнений по всем компонентам, входящим в кинетические уравнения. В результате была получена следующая система уравнений:
dCA |
1 k |
|
1 |
|
|
|
|
|
|
1 |
|
1 |
|
|
|
|
|
|
1 |
|
|
|||||||
C 4 |
C |
|
|
|
C 4 |
|
k |
|
|
C 4 |
|
|
||||||||||||||||
|
d |
|
|
4 |
1 |
|
A |
|
|
F |
|
N |
|
4 |
|
|
2 |
|
|
K |
|
(256a) |
||||||
1 k |
|
|
|
|
|
1 |
1 |
|
|
|
1 |
|
|
2 |
|
|
|
|
|
1 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
C |
|
C |
3 |
C 3 |
|
|
k |
C 3 |
|
C 3 |
; |
|
|
||||||||||||||
3 |
|
7 |
|
|
P |
K |
A |
|
|
|
3 |
8 |
|
БПФ |
|
|
|
|
FN |
|
|
|
||||||
|
dCF |
|
|
|
|
1 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
|
1 |
|
|
|
|
|||
|
k |
C 4 |
C |
F |
C 4 |
k |
2 |
C |
4 |
; |
|
|
(256б) |
|||||||||||||||
|
d |
|
|
1 |
|
A |
|
|
|
|
N |
|
|
|
|
|
K |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
dCN |
|
|
|
|
1 |
|
|
1 |
|
|
|
|
|
|
1 |
|
1 |
|
|
|
|
|
|
1 |
|
|
|
|
|
|
k |
|
C 4 |
|
C |
|
|
C 4 |
|
k |
|
|
C |
4 |
; |
(256в) |
||||||||||
|
d |
4 |
|
|
|
|
4 |
|
|
|||||||||||||||||||
|
|
|
|
1 |
A |
|
|
|
|
F |
N |
|
|
|
2 |
|
|
K |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
189 |
