
книги / Методы и автоматизированные системы аналитического контроля технологических процессов и окружающей среды. Методы и автоматизированные системы промышленного аналитического экологиче
.pdfСвет от источника резонансного излучения 1 пропускают через пламя, в которое впрыскивается мелкодисперсный аэрозоль 10 раствора пробы.
Излучение резонансной линии выделяют из спектра с помощью монохроматора 2 и направляют на фотоэлектрический детектор 3 (обычно фотоумножитель).
Выходной сигнал детектора после усилителя 4 регистрируют гальванометром 5, цифровым вольтметром или записывают в аналоговой форме на ленте пишущего потенциометра 6. Интенсивность резонансного излучения измеряют дважды: до распыления анализируемого образца в пламя и в момент его распыления. Разность этих двух отсчетов и определяет значение аналитического сигнала.
4.1.3. Эмиссионная фотометрия пламени
Метод эмиссионной фотометрии пламени основан на излучении энергии возбужденными атомами анализируемого вещества. Интенсивность испускания (эмиссии) излучения I пропорциональна концентрации определяемого компонента. Способы определения концентрации компонентов методом пламенной фотометрии аналогичны методам атомной абсорбции: метод сравнения, метод градуировочного графика и метод добавок (расчетный и графический).
4.1.4. Эмиссионный атомный спектральный анализ
Эмиссионные методы требуют воздействия на анализируемое вещество высокой температуры или, чаще, температуры и электрического поля (дугового или искрового разряда). При этом происходит испарение и диссоциация исследуемого вещества на атомы и ионы.
Атомы и ионы могут находиться в нормальном и возбужденном состояниях. В нормальном состоянии атомы (ионы) обладают минимальной энергией Е0. Под влиянием указанных выше воздействий происходит переход валентных электронов с нормального уровня на один из более высоких уровней Е1, Е2, …
71
По истечении ≈10–8 с возбужденный атом возвращается в нормальное или какое-либо промежуточное возбужденное состояние, например Е1. Освобождаемая при этом энергия ∆Е = = Е2 – Е1 излучается в виде кванта света hν:
∆Е = Е2 – Е1= hс/λ = hν,
где Е1, Е2 – энергия исследуемого и возбужденного состояний; h – постоянная Планка; с – скорость света; λ – длина волны излучения; ν – частота излучения.
Число энергетических переходов определяется строением электронных уровней каждого элемента. Каждому переходу соответствует определенная линия в спектре излучения.
По числу и положению линий в спектрах излучений определяют, какие элементы входят в состав анализируемого вещества, т.е. проводят качественный спектральный анализ.
Сравнивая интенсивность спектральных линий эталонов с интенсивностями тех же линий анализируемого вещества, определяют содержание элементов, т.е. выполняют количественный спектральный анализ.
Интенсивность спектральных линий I зависит от концентрации С элемента в пробе:
I =aCb или lnI = lna + blnC,
где а и b – константы.
Степень почернения (S) на фотопластинке, используемой для фотографирования спектра, соответствующая спектральной линии, определяется по формуле
|
I |
0 |
|
n |
0 |
|
|
S = ln |
|
|
= ln |
|
, |
||
|
|
|
|
||||
|
I |
|
|
n |
|
||
где I0 – интенсивность света, проходящего через фон пластинки; I – интенсивность света, прошедшего через спектральную линию на фотопластинке; п и п0 – соответствующие показания вторичного прибора, связанного с фотоэлементом.
Для определения концентрации элемента в пробе применяют метод градуировочной кривой (метод трех эталонов) или метод фотометрического интерполирования.
72

4.1.5. Методы люминесценции
Люминесценцией называют свечение атомов, молекул и других частиц, возникающее в результате электронного перехода при возвращении из возбужденного в основное (нормальное) состояние.
В зависимости от способа возбуждения частиц различают следующие виды люминесценции:
Способ возбуждения |
Вид люминесценции |
|
|
|
|
Электромагнитные излучения |
Фотолюминесценция |
|
(УФ, видимый спектр) |
||
|
||
Энергия химических реакций |
Хемилюминесценция |
|
Энергия химических реакций, |
Биолюминесценция |
|
протекающих в живых организмах |
||
|
||
Рентгеновское излучение |
Рентгенолюминесценция |
|
Электрическое излучение |
Электролюминесценция |
Из всех видов люминесценции наиболее часто используют фото- и хемилюминесценцию.
При прохождении потока света через раствор с концентрацией С часть потока поглощается, однако в люминесценцию преобразуется лишь часть поглощенного света, выражаемая квантовым выходом люминесценции. Интенсивность люминесценции Iл пропорциональна числу квантов люминесценции φл:
Iл = ϕ лIп ,
где Iп – интенсивность поглощения света, Iп=I0 – Il, I0 – интенсивность падающего света; Il – интенсивность света, прошедшего через слой толщиной l.
По закону Бугера
Il = I0e−ε λ lC ,
следовательно,
Iп = I0 − I0e−ε λ lC = I0 (1 − e−ε λ lC ) ,
73

Iл = ϕ лI0 (1− e−ε λ lC ) . |
|
Если произведение ε λ lC невелико (<< |
0,01), единицей |
в этом выражении можно пренебречь, тогда Iл |
= 2,3ϕ лI0ε λ lC . |
При постоянной длине кюветы с анализируемым веществом 2,3ϕ лI0ε λ l= const= k, отсюда Iл = kC.
Таким образом, при малых концентрациях вредных веществ в воздухе производственных помещений и воде производственного цикла наблюдается прямолинейная зависимость интенсивности люминесценции от концентрации.
Рис. 12. Схема хемилюминесцентного газоанализатора
В хемилюминесцентном газоанализаторе (рис. 12) анализируемый газ и воздух с постоянными объемными расходами из блока подготовки газов 1 поступают в реакционную камеру 2. Воздух предварительно проходит через озонатор 7, где под действием барьерного высоковольтного разряда в воздухе образуется озон. При взаимодействии в камере 2 озона с определяемым компонентом анализируемой смеси образуются продукты реакции в возбужденном состоянии. При переходе их
вустойчивое состояние происходит излучение квантов люминесценции. Электромагнитное излучение через окно 3 попадает
вфотоумножитель 4, сигнал которого преобразуется в унифицированный сигнал с помощью преобразователей 5. Выходной сигнал последнего воспринимается автоматическим потенциометром 6. При постоянной концентрации озона в воздухе, поступающем в камеру 2, интенсивность электромагнитного излучения пропорциональна концентрации определяемого компо-
74
нента в анализируемом газе. При такой подаче газов хемилюминесцентный газоанализатор может использоваться для селективного измерения микроконцентраций (в диапазонах от 0–10–5 до 0–10–4 об. % и более) непредельных углеводородов и оксидов азота. Он может применяться для селективного измерения микроконцентраций озона в воздухе. В этом случае воздух поступает в реакционную камеру 2, минуя озонатор, а вместо анализируемого газа в камеру с постоянным объемным расходом подается этилен.
4.2. Электрохимические методы
Из электрохимических методов в системе экологического мониторинга наиболее часто используют вольтамперометрию (включая полярографию), потенциометрию, кулонометрию и кондуктометрию.
4.2.1. Вольтамперометрия (полярография)
Вольтамперометрия включает в себя группу электрохимических методов анализа, основанных на изучении поляризационных кривых. Эти методы – полярография и амперометрическое титрование – имеют множество разновидностей и модификаций.
Наиболее распространена постоянно-токовая полярография. Полярографическая установка состоит из источника постоянного тока, делителя напряжения, капельного (обычно ртутного) электрода и вспомогательного (обычно ртутного) электрода. Для измерения силы тока в систему подключают микроамперметр. Электроды помещены вместе с исследуемым раствором в электролизере (ячейка) (рис. 13). Вольт-амперные кривые (полярограммы) получаются, если устанавливать различные напряжения на ячейку и измерять средний ток, проходящий через нее. На рис. 14 показана полярограмма однокомпонентного раствора. Она состоит из трех характерных участков: остаточного тока I, волны II и предельного тока III.
75
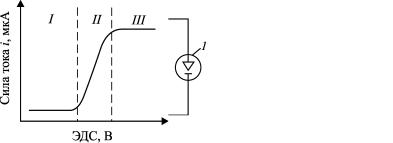
Рис. 13. Схема полярографической |
Рис. 14. Полярограмма |
установки: 1 – ячейкa; 2 – измеритель |
однокомпонентного |
тока; 3 – регулировочное |
раствора |
сопротивление |
|
В полярографии в качестве одного из электродов (поляризуемого) используют капли ртути, вытекающие из тонкого капилляра с одинаковой частотой. Благодаря этому поверхность электрода постоянно обновляется, раствор перемешивается в приэлектродном слое. Это позволяет получить воспроизводимые и надежные результаты.
Вкачестве другого электрода (неполяризуемого) используют обычно слой ртути на дне ячейки – «ртутное дно».
Основными характеристиками полярографа являются чувствительность и разрешающая способность. Под чувствительностью в полярографии понимают минимальную концентрацию, которую прибор может измерять с заданной точностью. Под разрешающей способностью понимают отношение концентраций сопутствующего (мешающего) и анализируемого компонентов. Полярографы обычно классифицируются по закону питания ячейки: классические полярографы, полярографы переменного тока, импульсные, высокочастотные, осциллографические полярографы.
Вклассической полярографии на ячейку накладывается медленно меняющееся поляризующее напряжение. Рассмотрим явления, происходящие на ртутно-капельном электроде.
76
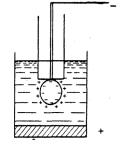
Пусть к ртутному дну присоединен плюс источника напряжения, а к ртутной капле – минус. Раствором служит электролит, содержащий ионы анализируемого вещества (рис. 15).
Наложенное на электролитическую ячейку напряжение вызывает поляризацию анода и катода:
E = φa – φк + iR,
где E – напряжение; i – сила тока; |
|
R – сопротивление раствора; φa и |
|
φк – потенциалы анода и катода. |
|
Если уменьшить сопротив- |
|
ление раствора, добавив сильный |
Рис. 15. Полярографическая |
электролит (фон), то величиной |
ячейка |
iR (падение потенциала в раство- |
|
ре) можно пренебречь. |
|
Потенциал анода практически остается постоянным во время работы электролизера, так как плотность тока мала и относительно большая поверхность анода не поляризуется. Тогда потенциал капающего поляризующего катода с небольшой по-
верхностью Е = –φк.
Часто в полярографических измерениях вместо слоя ртути на дне сосуда применяют неполяризующийся насыщенный каломелевый электрод, потенциал которого принимают равным нулю.
Полярографические данные получают путем измерения тока, проходящего через электролитическую ячейку, как функции потенциала, налагаемого на электроды. Графическую зависимость силы тока от потенциала называют полярографической волной (рис. 16).
В начале электролиза при небольших значениях наложенной ЭДС сила тока будет почти постоянной и лишь очень медленно возрастать. Это так называемый остаточный ток, который остается во все время электролиза. Как только будет достигнут потенциал восстановления ионов (например, для определяемых
77

ионов цинка он равен –1,0 В), начинается разряд их на капле ртути: Zn2++2e–+Hg→Zn(Hg).
На катоде образуется разбавленная амальгама цинка Zn(Hg), которая разлагается на ее составляющие, как только падающая капля соприкоснется санодом:
Zn(Hg) – 2e– →Zn2++Hg.
При потенциале восстановления ионов цинка сила тока резко возрастает (см. рис. 14), но после достижения определенной величины, несмотря на увеличение прило-
женной ЭДС, она остается почти постоянной. Этот ток называется предельным или диффузионным, его величина, как правило, пропорциональна концентрации определяемого вещества.
При снятии полярограмм к исследуемому электролиту добавляют какой-либо индифферентный электролит с катионами, восстанавливающимися гораздо труднее анализируемого катиона, например KСl, KNO3, NH4Cl, при концентрации, в 100–1000 раз превышающей концентрацию определяемого вещества. Такой электролит называют фоном. Его создают в исследуемом растворе для увеличения электропроводности с целью экранирования электрического поля индикаторного электрода (катода). Поэтому катионы определяемого вещества не притягиваются электрическим полем катода, адвигаются кнему засчет диффузии.
Важнейшей характеристикой полярограммы является потенциал полуволны Е1/2 и высота полярографической волны h (предельный диффузионный ток) (см. рис. 16). Потенциал полуволны используют в качественном полярографическом анализе. Потенциалы полуволны различных веществ, расположенные в порядке возрастания их отрицательного значения, составляют
78
так называемый полярографический спектр. Поскольку потенциал полуволны существенно зависит от состава раствора (анализируемой среды), в полярографических таблицах всегда указываетсяфон.
В количественном полярографическом анализе используют: метод градуировочного графика, добавок, сравнения, расчетный метод. При работе по методу градуировочного графика снимают полярограмму ряда стандартных растворов, устанавливают высоты волн (h) и строят градуировочный график в координатах высота волны – концентрация. Используя данный график, по высоте волны hх определяют искомую концентрацию Сх.
При работе по методу сравнения измеряют высоты волн на полярограммах двух-трех стандартных растворов и определяют средний коэффициент пропорциональности:
h1 = k1C1; h2 = k2C2; k1, k2 = const,
отсюда
k2 = h2 /C2; k1 = h1/C1; k = (k1 + k2)/2.
Далее, измерив высоту волны исследуемого раствора и использовав вычисленный коэффициент пропорциональности, определяют концентрацию Сx = hx/k.
В методе добавок измеряют высоту волны для исследуемого раствора h1, затем к нему добавляют строго определенное количество стандартного раствора СО и снова определяют высоту волны h2. Концентрацию определяемого элемента Сх находят решая систему уравнений:
h1 = kCx;
h2 = k(Cx + C0),
где (Cx + C0) – концентрация после добавления стандартного раствора; k – коэффициент пропорциональности.
Если известны коэффициенты диффузии D и характеристика капилляра, из которого вытекает ртуть (m2/3 t1/6), то концентрацию Cx определяемого загрязняющего элемента можно вычислить расчетным методом, используя уравнение Ильковича:
id = 607nD1/2m2/3t1/6Cx,
79

где id – диффузионный ток, мкА; n – число электронов, участвующих в электрохимической реакции; т – масса ртути, вытекающая из капилляра за 1 с, мг; t – время образования одной капли, с; Cx – концентрация, моль/дм3.
На рис. 17 приведена функциональная схема классического полярографа. Разрешающая способность полярографов классического типа порядка 50–100; чувствительность 10–3 моль/м3.
Среди различных вариантов полярографии метод дифференциальной импульсной полярографии (ДИП) наиболее эффективен для решения задач экологического мониторинга, главным образом благодаря высокой чувствительности. ДИП позволяет оценивать содержание всех веществ, определяемых методом классической полярографии. Среди других полярографических методов, удобных для следового ана-
лиза, квадратно-волновая полярография обеспечивает предел обнаружения, близкий к пределу обнаружения ДИП, но только в случае обратимых электродных процессов, и поэтому этот метод используется главным образом для определения следов тяжелых металлов. Метод ДИП может использоваться и для определения поверхностно-активных веществ, изменяющих емкость двойного электрического слоя электрода.
Для определения микросодержаний ионов тяжелых металлов могут быть использованы методы инверсионного электрохимического анализа (ИЭА), в которых определяемые металлы предварительно осаждают на электроде и затем растворяют при полярографическом контроле. Этот вариант в сочетании с ДИП
80
