
- •ЗАМЕЩЕННЫЕ КАРБОНОВЫЕ КИСЛОТЫ
- •КЛАССИФИКАЦИЯ. НОМЕНКЛАТУРА
- •В зависимости от положения дополнительной функциональной гр. по отношению к СООН-гр. замещенные карбоновые
- •ГАЛОГЕНОКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения α-галогензамещенные:
- •β-галогензамещенные:
- •Физические свойства
- •Реакции нуклеофильного замещения атомов галогенов
- •Реакции по карбоксильной группе:
- •ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения
- •Широко распространенные в природе α-гидроксикарбоновые к-ты могут быть
- •β-Гидроксикарбоновые кислоты получают:
- •γ- и -гидроксикарбоновые кислоты получают специальными методами.
- •Фенолкарбоновые кислоты синтезируют карбоксилированием фенолов.
- •Строение α-гидроксикарбоновые к-ты (кроме гликолевой НОСН2СООН) содержат асимметрический С-атом.
- •Физические свойства
- •Реакции по гидроксильной группе.
- •Реакции с участием ОН- и СООН- групп
- •γ- и δ-Гидроксикарбоновые к-ты при нагревании в кислой среде вступают в р-цию
- •α-гидроксикислоты при кипячении с разб. минеральными к-тами подвергаются расщеплению с образованием альдегидов и
- •Важнейшие представители
- •Гликозиды галловой кислоты – танины, содержатся в листьях чая, в кофейных зернах,
- •ОКСОКАРБОНОВЫЕ КИСЛОТЫ
- •Способы получения
- •– окислением α-гидроксикислот:
- •β-Оксокарбоновые к-ты могут быть получены гидролизом их сложных эфиров
- •Физические свойства
- •α-оксокислоты под действием разб. минеральных к-т декарбоксилируются с образованием альдегидов, а при действии
- •β-оксокислоты и их производные вследствие
- •β-оксокислоты и их соли термически нестабильные - легко распадаются при нагревании (декарбоксилируются).
- •Сложные эфиры β-оксокислот существуют в виде равновесной смеси двух таутомерных форм – оксо-формы
- •АУЭ является С-Н и О-Н кислотой средней силы, поэтому он реагирует с сильными
- •Соли АУЭ легко вступают в р-ции алкилирования и ацилирования,
- •Кетонное расщепление – осуществляют под действием кислот или разбавленных щелочей
- •Кислотное расщепление – осуществляется под действием конц. растворов щелочей и
- •Синтез кетонов и карбоновых кислот на основе АУЭ
- •Необходимо иметь ввиду:
- •Напр., рассмотрим схему синтеза пентан-2-она и бутановой кислоты.
- •Полная последовательность превращений:
- •кетонное расщепление
- •Важнейшие представители Пировиноградная кислота – бесцв. ж. с запахом уксусной кислоты.
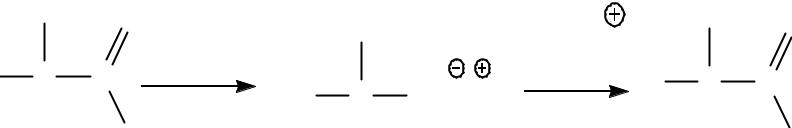
Реакции нуклеофильного замещения атомов галогенов
α, γ- и -Галогенокарбоновые к-ты реагируют
с нуклеофильными реагентами:
Br |
|
O |
|
|
OH |
|
|
OH |
O |
R C |
C |
NaOH, H2O |
|
|
|
H2O, H |
C |
||
|
|
R |
C |
COO Na |
|
R C |
|||
H |
|
|
- NaBr |
|
H |
|
|||
|
OH |
|
H |
|
|
OH |
|||
- |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
-гидроксикарбоновая |
||
бромокарбоновая |
|
|
|
|
|
||||
|
|
|
кислота |
|
|||||
кислота |
|
|
|
|
|
|
|||
Для β-галогенокарбоновых к-т характерны р-ции элиминирования с образованием α,β-ненасыщенных к-т, которые протекают одновременно с нуклеофильным замещением
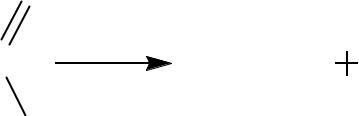
Реакции по карбоксильной группе:
образуют все функциональные производные карбоновых кислот (галогенангидриды, сложные эфиры и т.д.).
Декарбоксилирование
Особенно легко подвергаются декарбоксилированию α-тригалогенокарбоновые кислоты.
Oto C
X C |
|
C |
CHX3 CO2 |
X = Cl, Br |
|
||||
3 |
|
|
|
|
OH
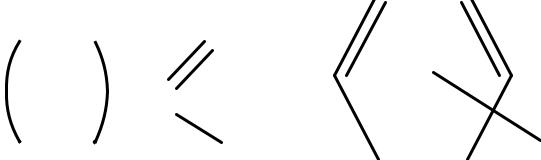
ГИДРОКСИКАРБОНОВЫЕ КИСЛОТЫ
- производные углеводородов, которые
содержат одновременно карбоксильные и гидроксильные группы
|
|
OH |
O |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
H |
|
|
|
|
|
|
|||
R |
|
C |
|
|
C2 |
|
C |
|
|
|
|
|
|
COOH |
|
|
|
H |
|
|
|
n |
OH |
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
n = 0,1,2,... |
|
|
|
|
|
|
|
||||
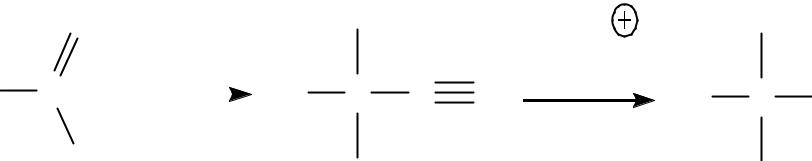
Способы получения
•Гидролиз галогенокарбоновых к-т (см. выше)
•Циангидринный метод:
O |
OH |
OH |
R C HCN, KCN |
R C C N HOH, H |
R C COOH |
R' |
R' |
R' |
Широко распространенные в природе α-гидроксикарбоновые к-ты могут быть
выделены из природного сырья. Этот метод позволяет получить
оптически активные продукты в отличие от синтетических методов получения таких кислот, когда продукты реакций представляют собой рацемические смеси.

β-Гидроксикарбоновые кислоты получают:
• по методу Реформатского (см. Тексты лекций)
• присоединением воды к α,β-ненасыщенным
кислотам
O |
H O, H SO |
4, |
100oC |
O |
|||||
|
|
|
|
|
|
||||
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
OH |
|
|
HO |
|
|
OH |
акриловая кислота |
|
|
3-гидроксипропановая кислота |
||||||
•гидролизом β-галогенкарбоновых к-т (см. выше);
•восстановлением β-оксокарбоновых к-т (см. ниже).

γ- и -гидроксикарбоновые кислоты получают специальными методами.
Дигидроксикарбоновые и дигидроксидикарбоновые к-ты получают окислением ненасыщенных кислот KMnO4 или
H2O2: |
|
|
|
COOH |
|
|
|
|
R |
|
|
|
|
H |
H |
||
|
|
|
|
KMnO4 |
|
|||
|
|
|
|
R |
|
|
COOH |
|
|
|
|
|
|
|
|||
H |
|
|
|
H |
|
|
||
|
|
|
|
|
||||
|
|
|
HO |
OH |
||||
|
|
|
|
|
||||
R = H, Alk, COOH
Фенолкарбоновые кислоты синтезируют карбоксилированием фенолов.
Напр., салициловые кислоты получают по методу Кольбе-Шмидта (см. «Фенолы»:
.
|
COONa |
|
ONa |
COONa |
|
OH |
||
CO2, tOC, p |
||
|
+ |
OH

Строение α-гидроксикарбоновые к-ты (кроме гликолевой НОСН2СООН) содержат асимметрический С-атом.
Природные α-гидроксикарбоновые к-ты подразделяются подобно моносахаридам на принадлежащие к D- и L- рядам:
HO |
|
O |
HO |
|
|
O |
|||
H |
|
|
|
OH |
HO |
|
|
|
H |
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
R |
||||
D-кислота L-кислота
Физические свойства
- бесцветные жидкости или кристаллические в-ва, растворимые в воде, кислые на вкус.
Химические свойства
Кислотность - более сильные кислоты, чем соответствующие незамещенные аналоги, т.к.
ОН группа обладает электроноакцепторным влиянием (–I эф.)
Реакции по карбоксильной группе. Гидроксик-ты
образуют все известные функциональные производные по СООН- гр. – соли, ангидриды, галогенангидриды, сложные эфиры и т.д.
