
лекции / Лекция 5
.pdfЛЕКЦИЯ 5
ГЕТЕРОГЕННЫЙ КАТАЛИТИЧЕСКИЙ ПРОЦЕСС
Катализ – это явление ускорения химической реакции под влиянием веществ, называемых катализаторами.
Действие катализатора заключается в том, что он открывает новый реакционный путь. Не входя в стехиометрическое уравнение реакции, катализатор многократно вступает в химическое взаимодействие с участниками реакции с образованием промежуточных соединений. Образование любого из промежуточных соединений требует меньшей энергии активации, чем при проведении реакции в том же направлении в отсутствии катализатора. Катализатор восстанавливает свой химический состав после каждого цикла промежуточных взаимодействий.
•катализОСНОВНЫЕможет бытьХАРАКТЕРИСТИКИиспользован для ускоренияКАТАЛИЗАвсех термодинамически возможных химических реакций;
•с помощью катализатора можно возбудить («разбудить») термодинамически возможные химические реакции, а не только ускорить;
•наличие промежуточного химического взаимодействия катализатора с реагирующими веществами при катализе;
•катализатор не расходуется в процессе реакции в отличие катализатор от инициатора. Инициатор гибнет в ходе реакции и при этом вносит свободную энергию своего превращения в химическую систему, инициируя цепь химических превращений, тогда как катализатор не вносит свою свободную энергию в систему (не совершает работу);
3
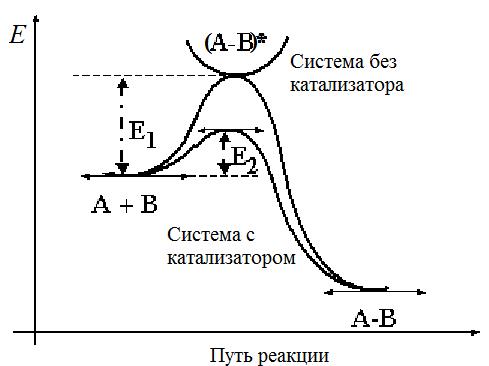
ИЗМЕНЕНИЕ ЭНЕРГИИ СИСТЕМЫ ПО РЕАКЦИОННОМУ ПУТИ
• Рисунок
КЛАССИФИКАЦИЯ КАТАЛИТИЧЕСКИХ РЕАКЦИЙ
по фазовым признакам каталитические реакции :
гомогенные,
гетерогенные
микрогетерогенные (ферментативные).
5
ПАРАМЕТРЫ ПОРИСТОЙ СТРУКТУРЫ
•Sуд − удельная внутренняя поверхность; на которой протекает реакция; значение Sуд для катализаторов составляет от 5 до
300 м2/г;
•− порозность − доля объема пор, через которые происходит
транспорт реагентов внутрь пористого зерна катализатора; обычно значение составляет 0,4−0,5;
•rп − средний радиус пор; его значения лежат в интервале 10− 100 нм.
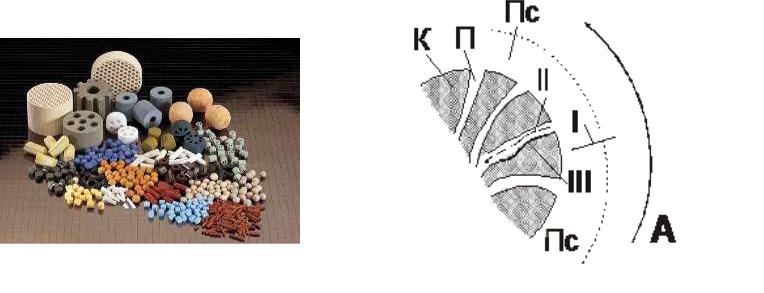
ГЕТЕРОГЕННЫЙ ПРОЦЕСС В ПОРИСТОМ КАТАЛИЗАТОРЕ
Схема и структура гетерогенно-каталитического химического
процесса:
К – катализатор П – поры катализатора
Пс – пограничный слой I, II, III – этапы процесса
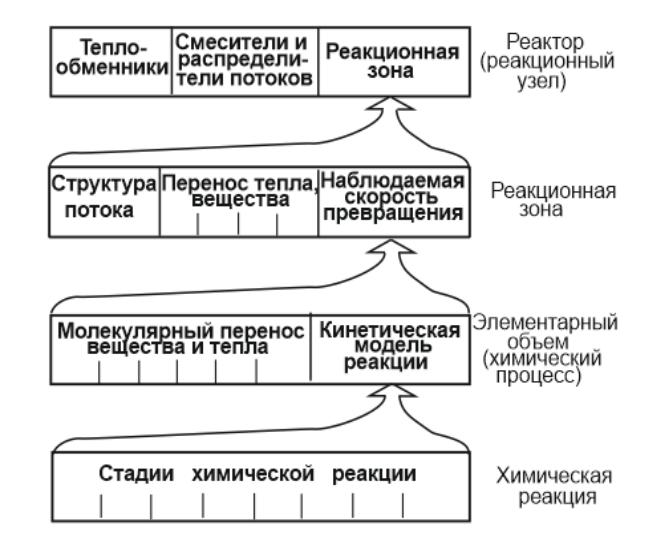
ИЕРАРХИЧЕСКАЯ СТРУКТУРА МАТЕМАТИЧЕСКОЙ МОДЕЛИ ПРОЦЕССА В РЕАКТОРЕ
8
МАТЕМАТИЧЕСКАЯ МОДЕЛЬ ПРОЦЕССА
• Допущения:
Форма зернаплоская пластинка толщиной 2R0;
Пластинка омывается с боковых сторон (площадь каждой S) газом с концентрацией реагента С0;
Пренебрегаем внешнедиффузионным торможением в связи с интенсивным внешним переносом;
Перенос А в порах характеризуется эффективным коэффициентом диффузии Dэфф;
Протекает реакция 1-го порядка А→R и W(С) = -kC ;
Условия процесса – изотермические и стационарные.
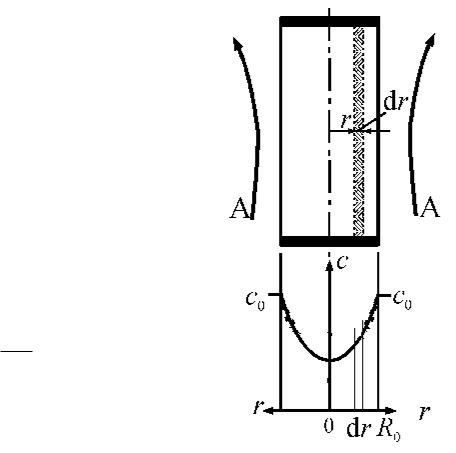
СХЕМА ПРОЦЕССА
•
•
•
•
•
•
•
•
Процесс симметричный, реагенты
диффундируют внутрь зерна, их концентрация снижается. Выделим плоский слой толщиной dr
и составим для него материальный баланс по А:
Изменение диффузионного потока равно скорости расходования А в выделенном слое:
|
|
|
|
или |
|
2 |
|
|
|
dc |
|
D |
d |
c |
кС 0. |
||
|
|
|
|
|||||
d DэфS |
|
|
WА Sdr |
|
эф |
dr |
2 |
|
|
dr |
|
|
|
|
|||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|||
Граничные условия: |
|
|
|
|
|
|||
при r = R0: |
C = C0. |
|
|
|
|
|
||
при r = 0: |
dC/dr = 0 |
|
|
|
|
|
||
