
органическая химия
.pdf
Органическая
химия
Органическая химия. Введение |
1 |

Предметомизучения органической химии являются органические соединения, структурную основу которых образуют атомы углерода.
Основныеатомы органогены: углерод С, водород Н, азот N,
кислород О, сера S, фосфор Р.
Главныезадачи органическойхимии, как науки:
1.Получение природных и синтез новых органических соединений с ценными свойствами (биоактивных веществ, лекарственных препаратов, красителей, пищевых продуктов, полимерных, композиционных и наноразмерных материалов и пр.).
2.Установление строения синтезированных и имеющихся в природе органических веществ.
3.Изучение закономерностей протекания и механизмов реакций органических соединений. Установление строения промежуточных частиц – интермедиатовреакций.
4.Внедрение достижений органической химии в практику
человеческой деятельности.
Органическая химия. Введение |
2 |
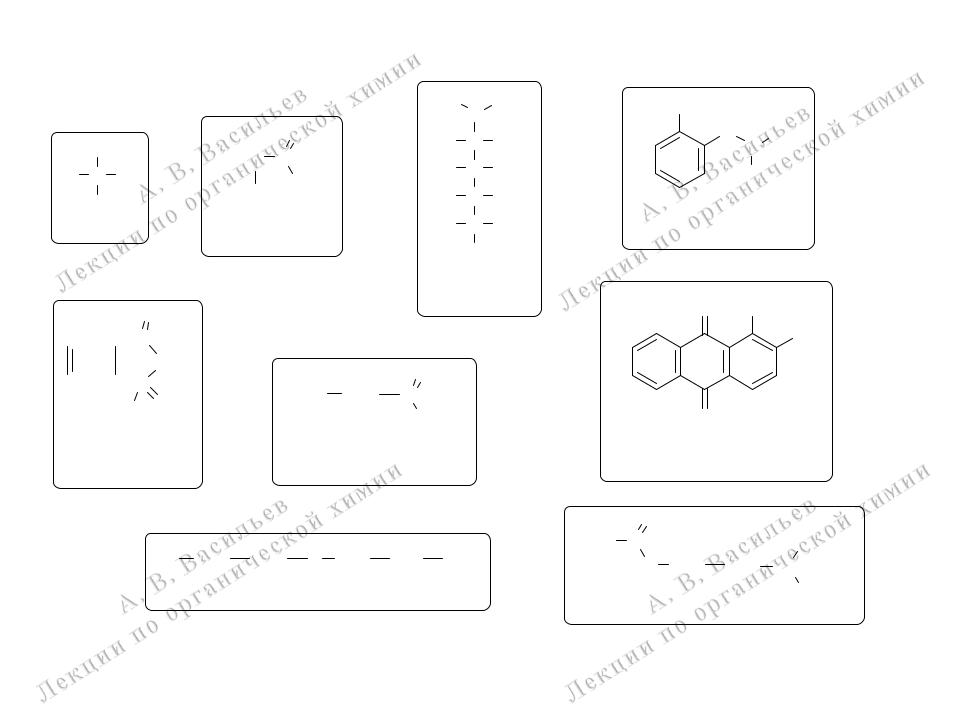
Примеры молекул органических веществ
H
H C H
H
метан
O 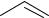
 C
C
NH
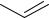
 S O
S O O
O
сахарин
(в 300 раз слаще сахара)
O
H2C C NH2 OH
глицин (аминокислота)
H3C CH2
H  O
O
C
H C OH
HO C H
H C OH
H C OH
CH2OH
D-глюкоза (углевод)
S O
O
C
H
пропантиаль-S-оксид (луковый запах)
Cl CH2 CH2 S CH2 CH2 Cl
иприт (боевое отравляющее вещество)
COOH
O  O
O
C
CH3
ацетилсаллициловая кислота (аспирин)
O OH
OH
O
ализарин (природный краситель)
O
H3C C |
CH3 |
O CH2 CH2 CH
CH3
изоамилацетат (грушевый запах)
Органическая химия. Введение |
3 |

Становление теории химического строения органическихсоединений
Конец XVIII – начало XIX вв. – период открытия и синтеза новых органических веществ (метана, этилена, ацетилена, бензола и др.)
1806 г. – И. Берцелиус определил органическую химию как химию соединений углерода.
1837 г. – теория радикалов Ж. Дюма и Ю. Либиха.
1851 г. – теория типов Ш. Жерара.
1861 г. – теория химического строения А.М. Бутлерова.
«Химическое строение – это порядок соединения атомов в молекуле»
А.М Бутлеров (1861 г.)
Александр Михайлович Бутлеров (1828-1886),
русский химик-органик. |
Органическая химия. Введение |
4 |

Основныепостулатытеории химического строения органических соединений
-атомы объединены в молекулы в строго определенной последовательности;
-атомы образуют четко определенное количество связей с соседними атомами, т.е. атомы характеризуются определенной валентностью (количеством образуемых связей), так в структурах органических молекул валентность углерода – 4, кислорода – 2, азота – 3, водорода – 1;
-органические вещества могут давать структурные изомеры – соединения, имеющие одинаковый состав атомов в молекулах, но различное строение;
-связанная определенным образом группа атомов составляет функциональную группу органического соединения и придает этому соединению характерные химические свойства.
Органическая химия. Введение |
5 |

Электронное строение атома углерода. Типы гибридизации атома углерода
Атом углерода С содержит 6 электронов.
переход электрона |
четыре неспаренных электрона - |
||||||||||||||||||||||
с 2s на 2р орбиталь |
валентность углерода четыре |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2p |
2p |
2p |
2p |
2p |
2p |
2s2 |
|
|
2s |
|
|
1s2 |
|
|
1s2 |
|
|
1s22s22p2 - основное электронное |
1s22s12p3 - возбужденное электронное |
состояние атома углерода |
состояние атома углерода |
Переход в атоме углерода одного электрона с 2s на 2р орбиталь приводит к появлению 4 неспаренных электронов, которые могут образовать 4 ковалентные связи с другими атомами.
Атом углерода является четырехвалентным!
Органическая химия. Введение |
6 |

sp3-Гибридизация атома углерода. Строение метана
2p 2p 2p
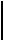 2s 1s2
2s 1s2 
s + 3 p
4 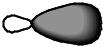
 sp3-гибридные орбитали
sp3-гибридные орбитали
H H
CH4 |
H C H |
H |
|
C |
|
H |
|
|
|
||||||
|
|
|
|
|
|
||
H H
s
 H
H
sp3 sp3 s
sp3 s  H
H C
C sp3
sp3
sp3 |
H |
H |
s |
s |
|
H
109o28' - тетраэдрический угол
H
 C
C H H
H H
Органическая химия. Введение |
7 |
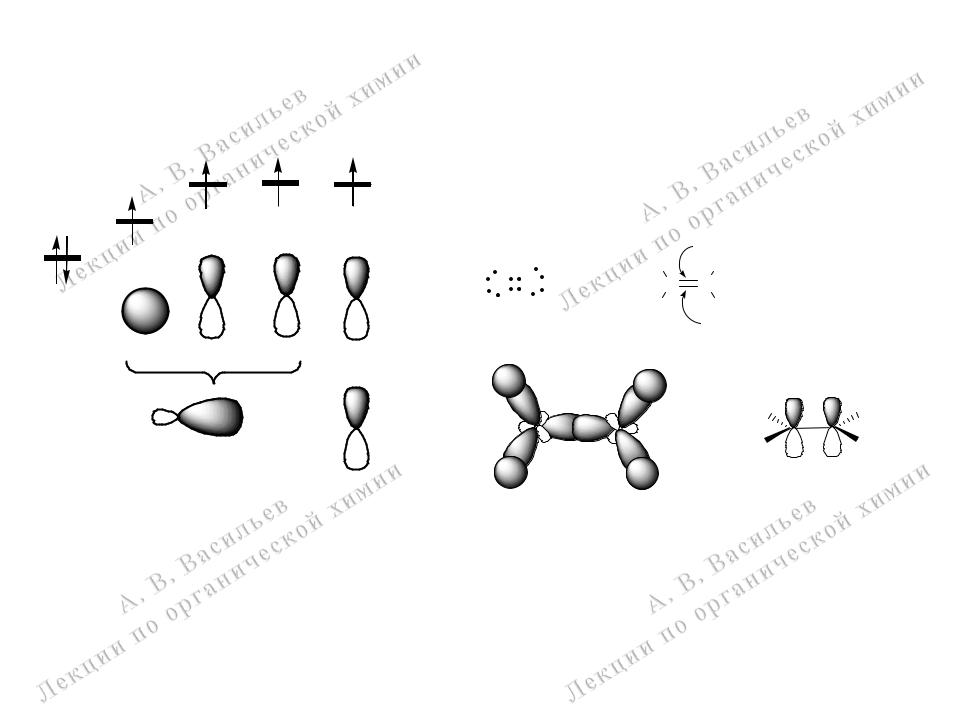
sp2-Гибридизация атома углерода. Строение этилена
2p |
2p |
2p |
|
|
|
|
-связь |
|
2s |
|
|
HC |
H |
|
H |
H |
|
|
|
C |
|
sp2C |
Csp2 |
|
||
1s2 |
|
|
H |
H |
|
H |
H |
|
s + |
2 p |
|
|
|
|
|
-связь |
|
|
s |
|
|
s |
|
|
||
|
|
|
H |
sp2sp2 |
|
H |
p |
p |
3 |
|
|
sp2 |
|
sp2 |
H |
H |
|
|
|
C |
|
|||||
|
|
|
sp2 |
C |
sp2 |
C |
C |
|
sp2-гибридные орбитали |
|
H |
H |
|||||
H |
|
|
H |
-связь - |
||||
|
|
p-орбиталь |
|
|
s |
перекрывание p-орбиталей |
||
|
|
|
s |
-связи, |
|
|
|
|
образуемые sp2-орбиталями
Органическая химия. Введение |
8 |
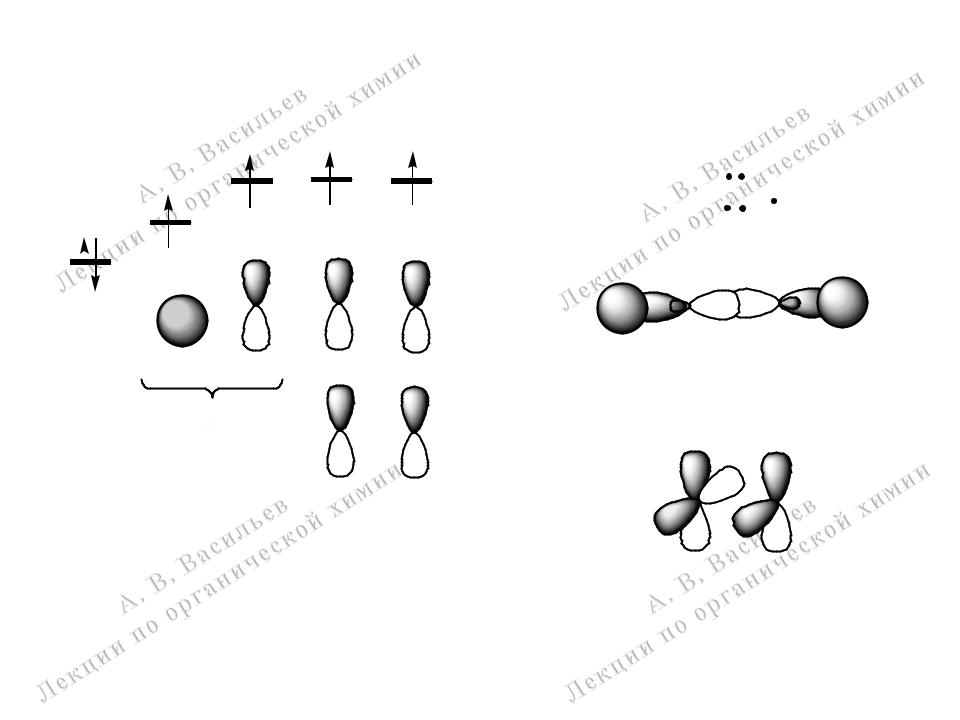
sp-Гибридизация атома углерода. Строение ацетилена
2p 2p 2p
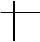 2s 1s2
2s 1s2 
s + p
2 

sp-гибридные
орбитали p-орбитали
H C
C
 C
C H
H
C C
H 
 H
H
-связи,
образуемые sp-орбиталями
p p
H C
C C
C H p p
H p p
-связи -
перекрывание p-орбиталей
Органическая химия. Введение |
9 |
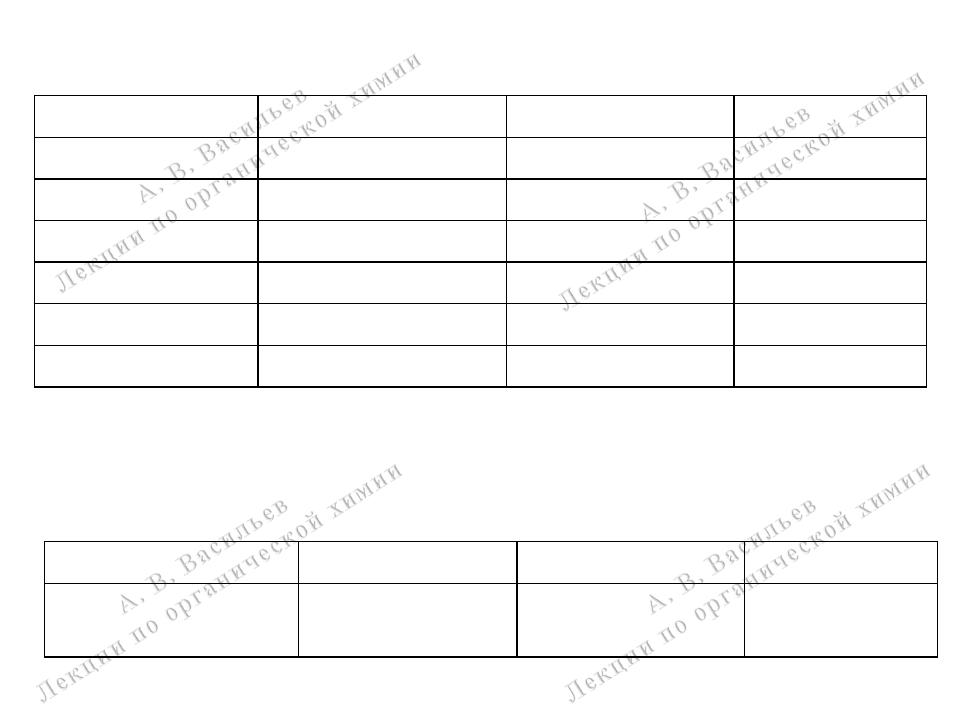
Длины связей в молекулах органических соединений
Связь |
Длина, нм |
Связь |
Длина, нм |
Сsp3–Csp3 |
0.154 |
Сsp3–H |
0.111 |
Сsp2=Csp2 |
0.134 |
Сsp2–H |
0.110 |
Сsp Csp |
0.120 |
Сsp–H |
0.108 |
С=O |
0.122 |
O–H |
0.096 |
Сsp2=N |
0.130 |
N–H |
0.101 |
C N |
0.116 |
S–H |
0.134 |
Энергии углерод-углеродных связей в молекулах органических соединений
Связь |
Сsp3–Csp3 |
Сsp2=Csp2 |
Сsp Csp |
Энергия, кДж/моль |
347-356 |
611-632 |
837 |
(ккал/моль) |
(83-85) |
(146-151) |
(200) |
Органическая химия. Введение |
10 |
