
moskvich_fizika
.pdfЛЕКЦИЯ 17
ЭЛЕМЕНТАРНАЯ КИНЕТИЧЕСКАЯ ТЕОРИЯ ПРОЦЕССОВ ПЕРЕНОСА В ГАЗАХ
Настоящая лекция посвящена раскрытию сущности явлений переноса и нахождению количественных выражений для макроскопических коэффициентов переноса в плотных и ультра разреженных газах. Прежде чем приступить к изложению элементарной теории явлений переноса сконцентрируем свое внимание на рассмотрении столкновений молекул между собой. Именно эти микроскопические процессы играют определяющую роль в механизмах переноса молекулярных свойств, не только в газах, но также в жидкостях и твердых телах.
17.1. Столкновения молекул и их количественные характеристики
Столкновения частиц вещества друг с другом приводят к случайному изменению их кинетических энергий и, в конечном счете, к установлению равновесного распределения молекул по скоростям. Столкновения могут приводить и к другим последствиям. Например, в результате столкновения может произойти ионизация атома, химическая или ядерная реакции и многое другое. Если бы не было столкновений, то распространение запахов в воздухе и выравнивание температур в жидкостях и газах происходило бы практически мгновенно, ведь средние скорости теплового движения молекул равны сотням метров в секунду. В действительности при отсутствии конвективных потоков воздуха или жидкости продолжительность подобных процессов может составлять минуты и часы. Так же медленно происходит выравнивание скоростей макроскопического движения газа или жидкости посредством сил вязкости.
Медленность диффузии и аналогичных ей процессов объясняется тем, то в результате непрерывной череды соударений с другими частицами каждая молекула мечется туда и сюда и поэтому её продвижение вперед происходит не по прямой. Вспомните движение броуновской частицы. Траектория молекулы также изломана, как и линия, представленная на рис. 7.1. Для количественной характеристики интенсивности столкновений молекул используется четыре параметра:
1.Эффективное сечение молекулы σ.
2.Средняя длина свободного пробега молекул λ.
3.Среднее время между столкновениями τ.
4.Средняя частота столкновений ν.
Все эти параметры связаны между собой.
201
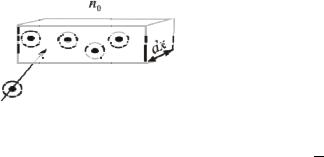
Эф фективное сече ие молекул
Обычно, при рассмотрении столкно вений одну частицу выделяют как движущ уюся, а все остальные счита тся неподвижн ыми частицамимишенями (рис. 17.1).
|
|
При таком подходе движение молекулы сле- |
||||||||||
|
|
дует характеризовать не средней скоростью |
|
от- |
||||||||
|
|
носител ьно стенок сосуда, а средней относительной |
||||||||||
|
|
скоростью |
отн |
|
двух произвольно взятых |
молекул. |
||||||
|
|
Прямое |
|
|
|
|
|
|
|
|
|
|
|
|
|
вычислен ие этой скорости с помощ ью рас- |
|||||||||
Рис. 17.1. |
пр еделения Максвелла дает результат: |
|
|
|
||||||||
|
|
|
отн |
√2 |
. |
|
|
|
|
|
|
|
Вероятность того, что движущаяся частица попадет в одну из частиц- |
||||||||||||
мишеней при прохождении слоя толщиной |
, пр опорциональна величине |
|||||||||||
, а так же концентрации молекул-мишеней |
: |
|
|
|
|
17.12 |
||||||
|
|
|
|
σ |
|
. |
|
|
|
|
|
|
Коэффициент пропорциональности |
|
имеет размерность площа ди (м ) и |
||||||||||
называется эффективным |
сечением |
молекулы. В общем случае |
|
|
, т.е. |
|||||||
|
|
|
σ |
|
|
|
нимости |
к моле- |
||||
зависит от энергии налетающей молекулы. В области приме |
|
σ σ |
ε |
|
||||||||
кулам к лассических моделей можно говорить, |
что завис ит от их средней |
|||||||||||
относительной скорости движения. Таким |
образом, формула (17.1) о пределя- |
|||||||||||
|
|
σ |
|
|
|
|
||||||
ет вероятность столкновения с конкретным результатом, который зави-
сит от энергии соударяю щихся частиц.
При столкновении молекула может изменить направление своего движения, т.е. рассеяться. Может поглотиться, диссоциировать молекулу или ионизиро вать атом, с которыми она сталкивается. В с оответствии с эт им гово-
рят об эффективных сечениях рассеяния, поглощения, диссоциации, иони-
зации и пр.
В ядерной физике и физике элементарных частиц так же ши роко используется понятие эффективного сечения частицы по отношению к какомулибо процессу. С ильная зависимость σ ε характерна для таких процессов как поглощение нейтронов атомными ядрами, деление тяжелых ядер под действием нейтронов, термоядерные реакции. Расчет эффективны х сечений таких процессов возможен на основе законов квантовой механики . Для процессов
переноса имею т значения только столкновения, привод ящие к упругому рассеянию молекул и ато мов на других мо лекулах и атомах. При эт ом внутреннее состояние сталкивающихся частиц не изменяется. Э ффективное сечение таких процессов слабо зависит от отн . Поэтому для его нахождения
202
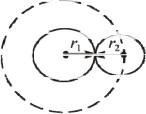
можно воспользоваться моделью твердых сфер и считать, что σ const. На рис. 17.2. изображены дв е шароподобные молекулы в момент их соударения.
Минимальное расстояние, на которое сбл ижаются центры двух тождественных молекул при столкн овении,
называются эффективным диаметром моле кулы
(рис. 17.2.). Площадь ограниченная пунктирной окруж-
ностью на рисунке равна эффективному сечению моле-
Рис. 17.2. кулы :
σ |
σ |
π . |
17.2 |
Если сталкивающи еся молекулы не тождественны, то |
17.3 |
||
σ |
π |
. |
|
Параметр σ так же называют газокинетическим эффективным сечением молекулы. Обратите вним ание, что модель жестких сфер использовалась Ван- дер-Ваальсом для описания отталкивания в реальном газе, но у Ван-дер- Ваальса были е ще и сил ы притяжения меж ду молекулами. Таким образом, в допущении σ const таи тся модель идеального газа. Сёзерленд в 18 93 году учел силы притяжения, с которыми молекулы действуют друг на друга в промежутках между столкновени ями. Он пришел к выводу, что сил ы притяжения, сближая молекулы, пролетающие мимо друг друга, делают возможными те столкновения, которые без притяж ения не случились бы. Это приводит к ув еличению σ.
Роль притяжения проявляется при малых относительных скоростях движения молекул, т.е. при низки х температурах. Экспери менты обнаруживают некоторое уменьшение эффективного сечения молекул с росто м температуры. В своей теории Сёзерленд получил формулу, носящ ую его имя, для среднего эффективного сечения молекулы реального газа
|
σ |
|
|
σS |
σ 1 |
|
, |
|
|
|
|
|
|||||
где, |
вычисляется согласно выражению (1 7.2), а – постоянная, называемая |
|||||||
|
||||||||
постоянной Сёзерленда. |
|
|
|
|
||||
|
|
Средняя длина свободного пробега молекул ы |
||||||
|
|
Продолжим |
анализ |
формул ы |
(17.1). |
Вероятность столкновен ия, как |
||
можно заметить, |
растет |
пропорционально пройденному мол екулой п ути . |
||||||
203

Длина пути λ, при которой эта вероятность равна единице, называется сред-
ней длиной свободного пробега молекул.
Согласно (17.1) получаем равенство
1 σ λ, |
17.4 |
из которого следует, что
λ |
1 |
17.5 |
σ . |
Формула (17.5) справедлива, если система состоит только из тождественных молекул. Если молекулы в системе разные, то надо учесть вероятность столкновений, как тождественных молекул, так и разных молекул друг с другом. В этом случае
|
|
λ σ |
|
λ σ |
|
1, |
|
|
|
|
λ σ |
|
λ σ |
|
1, |
|
|
|
|
λ |
σ |
1 |
σ |
, |
|
|
Здесь |
|
λ |
σ |
1 |
σ |
. |
|
|
и |
- концентрации молекул двух компонент; |
; |
и |
|||||
–средняя длина свободного пробега молекул компоненты 1σи |
компоненты |
|||||||
σ |
λ |
|||||||
2 соответственно.
Кинематические параметры и
Из определения параметров σ и λ естественным образом определяются параметры τ и ν. Действительно среднее время между двумя столкновения-
ми – это путь, деленный на среднюю скорость:
|
λ |
|
λ |
|
|
τ |
|
√ |
2 |
. |
17.6 |
отн |
|||||
Тогда средняя частота столкновений будет равна
ν |
1 |
√ |
2 |
. |
17.7 |
τ |
|
λ |
204

Сделаем количественную оценку четырех кинематических параметров на примере молекулярного азота при нормальных условиях, т.е. в приближении идеального газа:
|
σ 3,14· 2·10 |
м |
10 |
м ; |
м; |
||
Здесь |
λ 10 |
м ·2,7·10 |
м |
|
3·10 |
||
|
|
3·10 |
м |
|
|
2,7·10 |
м ; |
|
использовалось число Лошмидта |
|
|
|
|||
|
τ |
5·10 м/с |
6·10 |
с; |
|
||
|
ν |
1 |
|
1,6·10 с . |
|
||
|
6·10 |
с |
|
||||
После рассмотрения характеристик столкновений молекул нашей ближайшей задачей будет установление связи между макроскопическими коэффициентами переноса в идеальном газе с его кинематическими параметрами.
17.2. Обобщенное уравнение переноса
Решение поставленной задачи будет базироваться на выводе обобщенного уравнения переноса. Используемый для этой цели метод средней длины свободного пробега является оценочным. Главное достоинство такого подхода состоит в его простоте и акценте на физической сущности явления. Ожидаемые результаты могут отличаться от точных числовыми коэффициентами. Точные решения следуют из кинетического уравнения Больцмана.
Вывод обобщенного уравнения процесса
Описание системы
Рассматриваемая система – идеальный газ в слабо неравновесном состоянии. характеризует некоторое молекулярное свойство, отнесенное к одной молекуле газа (энергия, импульс, концентрация, электрический заряд).
– функция координаты, медленно изменяющаяся вдоль одного направления, например , но не зависящая от времени.
Актуальные свойства модели процесса
• При наличии градиента будет происходить движение или перенос в направлении его уменьшения.
• Перенос осуществляется встречными молекулярными потоками. Плотность этих потоков описывается известным уравнением эффузии
205

.
• Функциональная зависимость G(x) не известна.
• Чтобы восполнить этот пробел воспользуемся разложением в ряд Тейлора в окрестности некоторой точки. В качестве малого параметра можно взять любую величину : λ. Неравенство приведет впоследствии к неопределенности числового множителя в уравнении переноса.
Постановка задачи
Требуется получить обобщенное уравнение переноса на основе микроскопических представлений.
|
Вывод уравнения |
• Величину. |
малого параметра обычно берут равной λ, λ, λ,… Пусть |
• Изобразим встречные молекулярные потоки на схематическом рисунке (рис. 17.3), где ось направлена вдоль градиента .
|
|
|
λ/2 |
|
|
Рис.17.3. |
|
|||
• |
можно |
|
достаточно мала, поэтому |
на таком расстоянии от 0 |
||||||
Величина |
|
|||||||||
|
|
представить в виде: |
|
|
λ |
|
||||
|
|
|
|
λ |
0 |
|
. |
|||
|
|
|
|
2 |
|
|
2 |
|
||
206

• Тогда, плотность потока |
|
|
в направлении отрицательных значений |
||||||||||
оси Х запишем как |
|
|
|
1 |
0 |
|
λ |
|
|
|
. |
||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|||||||||
Плотность потока |
в |
направлении положительных значений оси |
|||||||||||
|
4 |
|
2 |
|
|
|
|
||||||
равна |
|
|
1 |
|
0 |
λ |
|
|
. |
||||
|
|
|
|
|
|
||||||||
|
|
|
4 |
|
2 |
|
|
||||||
• Суммарная плотность потока в положительном направлении оси Х :
|
|
|
|
1 |
λ |
|
. |
17.8 |
|
|
λ/2 |
|
|
4 |
|
||||
лучается, |
коэффициент получается равным |
1⁄4 |
λ |
по- |
|||||
• При |
|
|
, а при |
|
|||||
|
что он равен |
. В этом и проявляется неопределенность |
|||||||
(приближенность) |
метода средней длины свободного пробега. Точное |
||||||||
|
1⁄2 |
|
|
|
|
|
|||
значение числового коэффициента находится из кинетического уравнения Больцмана и равно 1/3, учитывая это, запишем:
1 |
λ . |
17.9 |
3 |
Это и есть обобщенное уравнение переноса.
17.3. Элементарная кинетическая теория теплопроводности, самодиффузии и вязкости плотных идеальных газов
Получим уравнение теплопроводности, самодиффузии и вязкости, исходя из обобщенного уравнения переноса (17.9).
1. Пусть переносимым молекулярным свойством является внутренняя энергия идеального газа, приходящегося на одну молекулу:
µµ
.
В этом случае обобщенное уравнение переноса переходит в уравнение теплопроводности
207

1 |
|
ρλ |
уд |
. |
17.10 |
||
|
3 |
|
|
|
|||
Выражение перед в (17.10) и есть коэффициент теплопроводности |
|
||||||
χ |
1 |
λ |
ρ |
уд. |
|
17.11 |
|
Формула (17.7) выражает зависимость теплопроводности от микроскопиче- |
||||||
|
|
3 |
ρ |
и уд. За- |
||
ских параметров и , а также от макроскопических параметров |
||||||
висимость от температуры определяется средней скоростью |
|
, т.е. |
||||
|
λ |
|
|
|
|
|
|
/ . Какχ видим, зависимость от температуры достаточно слабая и |
|
ре- |
|||
|
при |
|||||
шении некоторых задач можно пользоваться приближением, что |
|
|
||||
χ~ |
. А вот от давления теплопроводность плотных газов не зависит и |
|||||
|
|
|
|
|
χ |
|
const
не приближенно, а точно.
В этом легко убедиться. При фиксированной температуре в выражении
(17.11) от концентрации частиц зависят два множителя: |
λ~ |
и ρ~ |
. Эти |
|||||
зависимости аннулируют друг друга. |
|
|
|
|||||
Для газов при нормальных условиях |
χ |
лежит в интервале |
10 |
10 |
||||
2. Пусть |
χ |
0,17Вт/м · с; χ |
0,02Вт/м · с |
. |
|
|||
Вт/м·с. Например, |
|
|
|
|
||||
переносимое молекулярное свойство – концентрация «меченных» атомов, приходящаяся на одну молекулу фона:
.
В этом случае обобщенное уравнение переноса переходит в уравнение самодиффузии
1 |
λ . |
17.12 |
3 |
Выражение перед в (17.2) представляет коэффициент самодиффузии
1
3λ . 17.13
Как видим явно зависит только от микроскопических параметров. Зависимость от температуры и давления газа «зашита» внутри этих параметров.
208

Поскольку |
. |
~ |
/ , то и |
~ |
/ . В свою очередь |
~ |
~ |
, соответствен- |
|
но и |
~ |
|
Для газов при нормальных условиях |
~10 |
м /с |
||||
|
|
|
|
. |
|||||
3. Пусть переносимое молекулярное свойство - это импульс упорядоченного движения одной молекулы:
.
В этом случае обобщены уравнение переноса переходит в уравнение внутреннего трения или вязкости
|
|
|
|
1 |
ρλ |
|
. |
17.14 |
||
|
|
|
|
|
||||||
Следовательно, коэффициент |
вязкости |
η |
равен |
|
|
|||||
|
3 |
|
|
|
|
|
|
|||
|
|
η |
1 |
λ |
ρ. |
17.15 |
||||
Функциональная зависимость |
|
от3 |
температуры и давления подобна за- |
|||||||
висимости теплопроводности от |
этих параметров. Порядок величины |
|
в га- |
|||||||
|
η |
|
|
|
Па·с. |
η |
|
|||
зах при нормальных условиях составляет |
|
|
|
|||||||
Вы без особого труда |
самостоятельно можете получить формулы, вы- |
|||||||||
|
|
|
|
10 |
|
|
|
|
|
|
ражающие один коэффициент переноса через любой другой. Это дает возможность из исследования только какого-то одного явления переноса получить информацию о других процессах переноса. Экспериментальные измерения макроскопических коэффициентов переноса и полученные для них выражения в рамках кинетической теории (17.10), (17.13) и (17.15) позволяют оп-
ределить такие микроскопические параметры как |
, |
|
и . Подобные экспе- |
|
риментальные задачи включены в программу |
практикума по молекулярной |
|||
|
λ |
σ |
|
|
физике.
Физическая сущность таких явлений как теплопроводность и вязкость состоит в том, что в процессе столкновений молекул энергия теплового движения (теплопроводность) и импульс упорядоченного движения (вязкость) передаются от частицы к частице, от слоя к слою как эстафетная палочка. Несмотря на то, что частицы пребывают в хаотическом движении и беспорядочной толкотне, возникает упорядоченное движение определенного молекулярного свойства – поток энергии или поток импульса.
17.4. Явления переноса в ультраразреженных газах
Состояние разреженного газа называют вакуумом. Степень разрежения характеризуют тремя параметрами: ,λ и . Понятие вакуума относительно, чем больше размеры области, тем при меньшем давлении он достигается. В
209

теоретических рассмотрениях обычно используется сравнение величины λ с линейным размером сосуда , ограничивающего объем газа. Принято различать четыре степени вакуума. Признаки градации и соответствующие названия вакуума приведены в табл. 17.1.
|
Таблица. 17.1. |
|
|
Степени разрежения газа |
|
Соотношение λ и |
|
Вакуум |
|
λ |
низкий |
λ~ |
средний |
λ |
глубокий (высокий) |
λ |
ультраразреженный (сверхвысокий) |
Для описания явлений переноса наиболее «прозрачным» является случай ультраразреженного газа. Поскольку в этих условиях столкновения между молекулами практически отсутствуют, то и «эстафетный» механизм передачи молекулярных свойств не работает. Молекулы по прямым линиям летят от одной стенки сосуда к другой и обмениваются с ними, например, энергией (это уже не теплопроводность, а теплопередача) или импульсом упорядоченного движения (трение при малых давлениях). Механизмы переноса можно легко смоделировать, используя уравнение эффузии.
Одной из особенностей высокого вакуума является невозможность возникновения в нем конвекционных потоков. Наиболее трудным для теории является случай среднего вакуума, когда λ~ .
Трение и теплопроводность ультраразреженных газов
Независимость коэффициентов внутреннего трения и теплопроводности от давления газа, обоснованная нами в 17.3. имеет место при таких давлениях, когда λ . В сильно разреженных газах, как отмечалось выше, механизм трения совершенно иной, нежели в плотных газах. Изменение импульсов молекул происходит только при ударах о стенку сосуда, поэтому трение становится не внутренним, а внешним. Внешнее трение зависит от числа ударов о стенку, которое пропорционально концентрации частиц, а следовательно, и давлению газа.
Аналогичное заключение можно сделать и по поводу теплопередачи. Молекула как пчела, несущая нектар, летит от горячей стенки к холодной и
210
