
541
.pdf
жащаяся в этих соках липаза вызывает в слабощелочной среде гидролитическое расщепление триглицеридов.
В переваривании жиров важное значение имеют желчные кислоты, выделяемые печенью в составе желчи. По химическому строению желчные кислоты являются производными холановой кислоты.
холановая кислота К желчным кислотам относятся: холевая (3, 7, 12 три-
гидроксихолановая кислота), дезоксихолевая (3, 12 дигидроксихолановая кислота), хенодезоксихолевая (3,7 дигидроксихолановая кислота), литохолевая (3 гидроксихолановая кислота). Желчные кислоты находятся в желчи в виде парных соединений с гликоколом (H2NCH2COOH) и таурином (H2NCH2 CH2SO3H): гликохолевая, таурохолевая и т.д.
гликохолевая кислота
121

Таурохолевая кислота
Желчные кислоты выполняют три функции:
1)эмульгируют жиры;
2)активируют фермент липазу;
3)способствуют всасыванию жирных кислот – продуктов гидролиза жира.
Липаза вырабатывается панкреатической железой в малоактивной форме. Поступая в полость кишечника, она быстро активируется желчью.
Эмульсия жира гидролизуется действием активной липазы ступенчато. Сначала расщепляются внешние сложноэфирные связи (ά-эфирные связи) и образуется диглицерид и жирная кислота, затем отщепляется жирная кислота, стоящая
уβ-углеродного атома глицерина и образуется моноглицерид.
|
|
О |
|
|
|
О |
|
// |
|
// |
|
||||
(γ)СН2–О–С–R3 |
|
СН2–О–С– R3 |
липаза |
||||
|
|
О |
|
|
|
О |
→ |
|
|
|
|
||||
|
|
// |
липаза |
|
|
// |
+НОН |
|
|
||||||
(β)СН – О – С – R2 |
→ |
СН – О – С – R2 |
|
||||
|
|
|
+НОН |
|
|
|
|
|
|
|
|
|
|
|
|
(α)СН 2 – О – С – R1 |
|
|
|
СН 2 ОН + R1СООН |
|||
\\ |
|
|
|
|
|
||
|
|
О |
|
диглицерид жирная кислота |
|||
триглицерид |
|
|
|
|
|
||
|
|
|
|
122 |
|
|
|
|
О |
|
|
|
|
|
// |
|
|
|
|
СН 2 |
– О – С – R3 |
СН 2 |
ОН + R3СООН |
||
|
|
|
|
||
│ |
|
липаза |
|
|
жирная кислота |
СН –ОН + R2СООН |
→ СН ОН |
||||
│ |
жирная кислота |
+НОН |
|
|
|
|
|
||||
СН 2 |
ОН |
|
|
СН 2 |
ОН |
|
|||||
моноглицерид |
глицерин |
||||
4.2.1. Ферментный гидролиз жира
Реактивы: гидрокарбонат натрия 1н раствор; желчь; поджелудочная железа; фенолфталеин 0,1% раствор; растительное масло.
Приборы: колбочки на 50 мл, пипетки, бюретка, водяная
баня.
Ход работы.
В колбочку вносят 1 мл растительного масла, 10 мл воды, 10 капель желчи,1–2 капли фенолфталеина и столько капель 1 н гидрокарбоната натрия, чтобы жидкость приобрела хорошо заметное розовое окрашивание (слабощелочная реакция). Затем вносят кусочек свежей поджелудочной железы (проба 1).
Параллельно ставят такой же опыт, но без желчи (проба 2) и еще опыт с желчью, но без поджелудочной железы (про-
ба 3).
Все три колбочки помещают в водяную баню, нагретую до 38°С. Через 20 минут колбочки достают из бани и отмечают, где произошло обесцвечивание раствора.
Суть опыта состоит в том, что при гидролизе жира липазой образуются глицерин и жирные кислоты, которые смещают реакцию среды в кислую сторону (розовое окрашивание исчезает). В колбочках, в которых произошло обесцвечивание, титруют 1 н гидрокарбонатом натрия до слаборозовой окраски. Результат титрования заносят в таблицу 4.1.
123
Таблица 4.1
Результаты опыта
Растворы |
|
Проба |
|
|
1 |
2 |
3 |
|
|
|
|
Растительное масло, мл |
1 |
1 |
1 |
Вода дистиллированная, мл |
10 |
10 |
10 |
Желчь, капли |
10 |
- |
10 |
Фенолфталеин, капли |
2 |
2 |
2 |
NaHCO3, 1н по каплям |
до розового окрашивания |
||
Поджелудочная железа, г |
1 |
1 |
- |
Температура (20 мин.) |
38° |
38° |
38° |
Цвет раствора |
|
|
|
Идет ли гидролиз жира |
|
|
|
Количество 1н NaHCO3, пошедшее на |
|
|
|
титрование, мл |
|
|
|
По результатам титрования сделать вывод, ответив на вопросы:
1.В какой колбочке прошел лучший гидролиз жира и почему?
2.Где идет замедленный гидролиз и почему?
3.В какой колбочке не происходит гидролиз жира и почему?
4.Какова роль желчи в переваривании жира?
Написать реакцию ступенчатого гидролиза сложного триглицерида, в состав которого входят линолевая, пальмитиновая и арахидоновая кислоты.
4.2.2. Цветная реакция на желчные кислоты
Реактивы: желчь; сахароза 5% раствор; серная кислота концентрированная.
Приборы: пробирки, пипетки. Ход работы.
В пробирку вносят 3 мл разбавленной вдвое водой желчи, прибавляют 3 капли 5% раствора тростникового сахара, взбалтывают и осторожно приливают по стенке пробирки равный объем концентрированной серной кислоты.
Через пару минут перемешивают содержимое пробирки встряхиванием, охлаждают ее под краном водопровода и,
124
закрыв пробкой, энергично взбалтывают. Жидкость и пена над ней окрашиваются в характерный пурпурный цвет.
Параллельные пробы с серной кислотой и желчью, но без сахара, или с серной кислотой и сахаром, но без желчи не дают пурпурного окрашивания.
4.2.3. Поверхностная активность желчи
Соли желчных кислот являются хорошими эмульгаторами. Как поверхностно-активные вещества они адсорбируются на поверхности жировых капель, снижая этим самым поверхностное натяжение на границе раздела двух фаз – воды и жира. Уменьшение поверхностного натяжения приводит к тому, что крупные капли жира становятся неустойчивыми и распадаются на ряд мелких капель. Образующаяся на жировых каплях тончайшая пленка из желчных кислот препятствует слиянию мельчайших капелек жира в более крупные капли.
Врезультате воздействия на жиры желчных кислот в кишечнике образуется очень тонкая стойкая эмульсия, диаметр частиц которой не превышает 0,5 мкм. Эмульгирование жира приводит к колоссальному увеличению поверхности жира, что способствует значительно большему контакту жиров с липазой и быстрейшему расщеплению жира.
Реактивы: желчь, растительное масло, серный цвет. Приборы: штатив с пробирками, пипетки.
Ход работы.
Вдве пробирки вносят по 1 мл растительного масла и по 10 мл воды. Затем в одну из пробирок прибавляют 10 капель желчи, обе пробирки одновременно энергично взбалтывают – пена и стойкая эмульсия наблюдаются только в пробирке, содержащей желчь.
Вдве пробирки вносят по 5–6 мл воды и по щепотке серного цвета. Затем в одну из пробирок прибавляют 5 капель желчи, и обе пробирки одновременно взбалтывают. Желчь как поверхностно-активное вещество, сильно понижает поверхностное натяжение воды, вследствие чего большая часть серы в пробирке, содержащей желчь, тонет, в то время
125
как в пробирке без желчи серный цвет плавает на поверхности воды.
4.2.4. Образование холеиновых кислот
Глицерин, возникающий при гидролизе триглицеридов, хорошо растворим в воде и легко всасывается слизистой оболочкой тонкого кишечника. Жирные кислоты в воде не растворимы, и в чистом виде всасываться не могут. Большую роль в их всасывании играют желчные кислоты. Жирные кислоты вступают в соединение с желчными кислотами, образуя растворимые комплексы, которые называются «холеиновые кислоты». Желчные и жирные кислоты входят в состав этих комплексов в различных соотношениях: 4:1; 7:2; 8:3; 9:4, т.е. на одну молекулу жирной кислоты приходится от двух до четырёх молекул желчных кислот. Такое соединение кислот придает им растворимость, и эти комплексы всасываются.
Внутри эпителиальных клеток кишечных ворсинок всосавшиеся холеиновые кислоты вновь распадаются на свои компоненты – желчные и жирные кислоты. Далее желчные кислоты поступают в воротную вену, печеночные капилляры, задерживаются в печени и снова переходят в состав желчи. Затем желчные кислоты вместе с желчью поступают в желчный пузырь, а оттуда вновь выводятся в кишечник. Происходит круговорот желчи, который имеет большое физиологическое значение. Такая циркуляция желчных кислот обеспечивает всасывание большого количества жира при сравнительно небольшой выработке печенью желчных кислот.
Реактивы: олеиновая кислота; натрия карбонат 2 н раствор; желчь.
Приборы: штатив с пробирками, пипетки. Ход работы.
Вдве пробирки, одна из которых содержит 5 мл желчи,
авторая – 5 мл Н2О, вносят по 1 мл олеиновой кислоты и по 5 мл 2н раствора карбоната натрия и энергично взбалтывают.
126
В пробирке без желчи образуется совершенно непрозрачная белая эмульсия (жирные кислоты не растворимы в воде), в то время как жидкость во второй пробирке становится прозрачной вследствие образования растворимых комплексных соединений желчных кислот с олеиновой (холеиновой) кислотой.
4.2.5. Реакция Сальковского на стерины
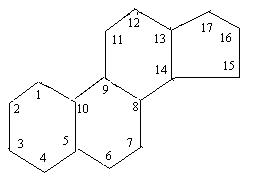
Стерины – высокомолекулярные циклические одноатомные спирты. В основе их лежит ядро циклопентанпергидрофенантрена, который можно рассматривать как продукт конденсации циклопентана и гидрированного фенантрена:
Циклический компонент стеринов построен из 17 атомов углерода. Стерины широко распространены в растительном и животном мире. Растительные стерины объединяют под названием «фитостерины», стерины животного происхождения называют «зоостерины», в грибах – «микостерины».
Одним из наиболее распространенных стеринов является холестерин и его производные – холестериды, которые являются сложными эфирами холестерина и высших жирных кислот. Холестерин – вторичный высокомолекулярный циклический спирт, производное циклопентанпергидрофенантрена, от семнадцатого атома которого отходит боковая цепь из восьми углеродных атомов, в циклическом компоненте имеется двойная связь между 5 и 6 атомами углерода, спиртовая группа находится у третьего атома углерода.
127

Холестерин
Производным холестерина является 7- дегидрохолестерин (провитамин Д3), который отличается от холестерина наличием второй двойной связи между 7 и 8 атомами углерода. 7-дегидрохолестерин содержится в коже животных, при облучении его ультрафиолетовыми лучами образуется витамин Д3.
Холестерин входит в состав каждой клетки животного организма (клеточные мембраны) в свободном виде или в соединении с белками. Особенно много холестерина содержится в белом веществе головного мозга, яичном желтке, сперме, желчи. В большом количестве он входит в состав жиропота овец. При промывке шерсти овец получают ланолин – густую, вязкую массу буро-желтого цвета нерастворимую в воде.
Холестерин является источником образования в организме ряда биологически активных веществ: желчных кислот, половых гормонов и гормонов коры надпочечников. Всех их объединяют в группу стероидных гормонов.
Реактивы: хлороформ; ланолин; серная кислота, концентрированная.
Приборы: штатив с пробирками, пипетки. Ход работы.
128
Несколько мг ланолина растворяют в 3 мл хлороформа, полученный раствор смешивают с равным объемом концентрированной серной кислоты, и смесь взбалтывают. Отстоявшийся слой серной кислоты окрашивается в виннокрасный цвет с зеленой флуоресценцией, в то время как хлороформовый слой приобретает оранжевую окраску, переходящую в кроваво-красную (рекомендуется дать смеси некоторое время постоять).
4.2.6. Окисление билирубина
Билирубин (красный) и биливердин (зеленый) являются продуктами распада гема в печени и селезенке, откуда они поступают в состав желчи, создавая зелено-бурую окраску. Поэтому билирубин и биливердин называют желчными пигментами.
При разрушении молекула гема теряет железо и одну из метиновых групп (=СН-), в связи с чем порфириновый цикл разрывается, и образуется открытая цепь, состоящая из четырех пирольных колец.
|
|
|
СООН СООН |
|
|
||
|
|
|
| |
| |
|
|
|
|
|
СН2 |
СН2 |
СН2 |
|
|
СН2 |
|
|
║ |
| |
| |
|
|
║ |
СН3 |
|
СН СН3 |
СН2 |
СН2 |
СН3 СН3 |
|
СН |
|
| |
| |
| |
| |
| |
||
НО- |
|
=СН- |
-СН- |
- |
-СН= |
|
-ОН |
|
|
||||||
|
N |
NH |
NH |
|
N |
||
|
|
|
Билирубин |
|
|
|
|
|
|
|
129 |
|
|
|
|
|
|
|
СООН СООН |
|
|
||||
|
|
|
| |
| |
|
|
|
|
|
|
|
СН2 |
СН2 |
СН2 |
|
|
|
СН2 |
|
|
|
║ |
| |
| |
|
|
|
|
║ |
СН3 |
|
СН СН3 СН2 |
СН2 |
СН3 СН3 |
|
СН |
|||
|
| |
| |
| |
|
| |
| |
|||
|
|
|
|
|
|
|
|
|
|
НО- |
|
=СН- |
-СН= |
|
--СН= |
|
-ОН |
||
|
|
|
|||||||
|
N |
NH |
|
N |
|
|
N |
||
|
|
|
Биливердин |
|
|
|
|
||
Реактивы: перекись водорода 3% раствор; 10% раствор аммиака; желчь.
Приборы: штатив с пробирками, пипетки. Ход работы.
3 мл желчи смешивают в пробирке с 1 мл 10% раствора аммиака, после чего вносят туда же 1 мл 3 % раствора перекиси водорода. После взбалтывания проследить за изменением окраски раствора. Сравнить с окраской желчи и сделать вывод.
Вопросы для самостоятельной работы:
1.Каково значение холестерина, его строение, биологическая роль?
2.Эргостерин, значение, строение, биологическая роль.
3.Какие существуют желчные пигменты?
4.3. Контрольные вопросы
1.Общая характеристика и биологическая роль липидов.
2.Какая существует классификация липидов?
3.Каково строение нейтрального жира? Характеристика высших жирных кислот. Структурные и запасные жиры.
130
