
6959
.pdfВеличину концентрации Н+ и рН измеряют при помощи приборов иономеров. рН-метр состоит из датчика и измерительного устройства. Датчик представляет собой своеобразный гальванический элемент: один электрод его имеет постоянное значение потенциала (электрод сравнения), величина потенциала второго электрода – функция концентрации одного из ионов раствора, в который погружены электроды. Этот электрод называют индикаторным (или измерительным). Электродвижущая сила (ЭДС) такого гальванического элемента – также функция концентрации ионов раствора, которые участвуют в возникновении скачка потенциала индикаторного электрода. Для измерения концентрации ионов Н+ в растворе в качестве индикаторного используют стеклянный электрод, т.к. потенциал его ( ст) зависит от концентрации Н+:
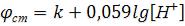 или
или
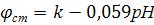 , где
, где
k – константа, зависящая от сорта стекла, из которого изготовлен электрод.
Экспериментальная часть.
1. Начертите таблицу 2.
Таблица 2
№ |
0,01М раствор |
рНэксп. |
[Н+] |
Уравнение |
рНтеор. |
|
|
|
|
реакции |
|
1. |
H2O |
|
|
H2O H+ + OH- |
|
2. |
NaCl |
|
|
|
|
3. |
HCl |
|
|
|
|
4. |
CH3COOH |
|
|
|
|
5. |
NH4Cl |
|
|
|
|
6. |
CH3COONH4 |
|
|
|
|
7. |
CH3COONa |
|
|
|
|
8. |
Na2CO3 |
|
|
|
|
9. |
NH4OH |
|
|
|
|
10. |
NaOH |
|
|
|
|
2.Настройте прибор в соответствии с инструкцией к нему (при настройке прибора консультируйтесь с дежурным лаборантом).
3.В 9 нумерованных стаканов налейте по 50 мл 0,01М растворов веществ, приведенных в таблице.
4.Измерьте рН дистиллированной воды. Значение запишите в таблицу 2.
5.Вынув электроды из сосуда с дистиллированной водой, просушите их кусочком фильтровальной бумаги и погрузите их в следующий раствор №2. Измерьте значение рН и запишите в таблицу 2.
6.Выньте электроды из раствора, промойте поверхность электродов дистиллированной водой из промывалки над стаканом «слив» и вновь просушите
фильтровальной бумагой. Сухие электроды погрузите в следующий раствор. Аналогичные операции повторите со всеми растворами.
7.После измерения рН последнего раствора электроды промойте и погрузите в стакан с дистиллированной водой. Выключите прибор из сети.
8.По значениям рН растворов рассчитайте концентрацию ионов Н+ в каждом растворе.
9.Рассчитайте и внесите в таблицу 2 теоретические значения рН растворов. Расчет рН растворов солей производят по формулам таблицы 1, а расчет рН растворов кислот и оснований, с использованием формул 1 – 9.
Выводы
1.Установлено, что в растворах солей среда (кислая, щелочная, нейтральная) . . .
2.рН растворов кислот HCl и CH3COOH резко отличаются при одной и той же концентрации электролита. Это объясняется тем, что . . .
Вопросы.
1.Почему в растворах хлороводородной и уксусной кислот одинаковой молярности концентрация ионов Н+ и рН различные?
2.Как объяснить разный характер среды в растворах используемых солей? Составьте уравнения реакции гидролиза этих солей.
3. Сделайте вывод об особенностях диссоциации сильных и слабых электролитов. Почему в таблице констант диссоциации (см. приложение) нет HCl, HNO3, HClO4, NaOH, КОН, а для Н2SO4, Ca(OH)2, Ba(OH)2 приведены лишь значения констант ионизации по второй ступени.
ТЕСТ 1
Процессы в водных растворах электролитов
1)В жидкой воде (обычно мы называем ее просто «вода») протекает процесс самоионизации. В результате в воде наряду с молекулами воды, их ассоциатами находятся ионы . . . и . . . равновесные концентрации которых равны………...
2)В чистой жидкой воде и водных растворах любого вещества при стандартной температуре произведение концентрации (точнее активностей) ионов гидроксония и гидроксила равно:
1. 10-7;
2.10-14;
3.1,8∙10-16.
3) Водородный показатель (рН) раствора рассчитывают по формуле:
1. 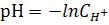
2. 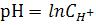
3. 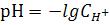
4. 
4) Для водных растворов справедливо соотношение: |
|
|
|||||||
|
1) рН + рОН = 7; |
|
2) рН + рОН = 14; |
||||||
|
|
3) рН рОН; |
|
|
4) рН рОН; |
|
|
||
5) В таблице приведены значения ионного произведения воды (КW) в |
|||||||||
зависимости от температуры: |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
t, С |
0 |
25 |
|
40 |
|
60 |
|
100 |
|
|
|
|
|
|
|
|
|
|
|
КW |
1,15∙10-14 |
1,00∙10-14 |
|
3,00∙10-14 |
|
9,50∙10-14 |
|
1,00∙10-14 |
|
|
|
|
|
|
|
|
|
|
|
Процесс самоионизации воды: |
1. Экзотермический; |
|
|
||||||
|
|
|
|
2. эндотермический; |
|
|
|||
При 60 С рН воды: |
1. равен 7; |
|
|
|
|
|
|
||
2.больше 7;
3.меньше 7.
6)Вещества, которые при растворении в воде или в расплавах образуют ионы, называют . . .
К ним относятся: 1. . . .
2. . . .
3. . . .
7) При растворении в воде кислот, оснований и некоторых солей равенство концентраций ионов Н+ и ОН- может нарушаться. Установите соответствие:
Раствор вещества |
рН раствора |
|
1. |
Кислота |
А. 7 |
2. |
Основание |
Б. 7 |
3. |
Соль |
В. = 7 |
8) Растворы, рН которых равен 7 называют . . . меньше 7 называют . . ., больше 7
– . . .
|
9) Слабыми электролитами являются: |
|
|
|
|
||
|
1) CrCl3; |
2) H2SO3; |
3) Cr(OH)3; |
4) NH4OH. |
|||
|
10) Слабым основанием является: |
|
|
|
|
||
|
1) NaOH; |
2) Ca(OH)2; |
3) Fe(OH)3; |
4) LiOH. |
|||
|
11) Сильными кислотами являются: |
|
|
|
|
||
|
1) НCl; |
2) H3РO4; |
3) HF; |
4) HI. |
|||
|
12) Установите соответствие: |
|
|
|
|
||
|
|
|
|
|
|
||
Водный раствор вещества |
|
рН раствора |
|
|
|
||
1. H2SO4 |
|
A. 7 |
|
|
|
|
|
2. |
(NH4)2SO4 |
|
|
|
|
|
|
3. K2CO3 |
|
Б. меньше 7 |
|
|
|
||
4. |
AlCl3 |
|
|
|
|
|
|
5. |
(NH4)2S |
|
В. больше 7 |
|
|
|
|
6. Na2S |
|
|
|
|
|
|
|
7. |
NaI |
|
|
|
|
|
|
8. |
KCl |
|
Г. близко к 7 |
|
|
|
|
9. NH4OH |
|
|
|
|
|
|
|
10. Ca(OH)2 |
|
|
|
|
|
|
|
|
13) Водородные показатели (рН) для растворов NH4OH (1) и NaOH (2) с |
||||||
одинаковой молярной концентрацией: |
|
|
|
|
|||
|
1. равны в обоих растворах; |
2. в растворе 1 больше чем в 2; |
|||||
|
3. в растворе 1 меньше чем в 2; |
4. нельзя определить. |
|||||
14) Приготовлены 0,01М растворы веществ. Установите соответствие:
0,01М раствор веществ |
рН |
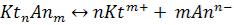
1. NaOH |
А. 2 |
|
2. NH4OH |
Б. 5 |
|
3. |
HCl |
В. 7 |
4. |
NaCl |
Г. 10 |
5. HCN |
Д. 12 |
|
15) Для расчета рН раствора слабой кислоты используют формулу:
1. 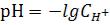
2. 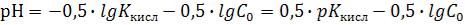
3. 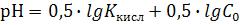
Где Ккисл – это . . .
рКкисл – это . . .
С0 – начальная концентрация кислоты.
16) В 0,01Н растворе одноосновной кислоты рН=4. Эта кислота:
1. сильная; |
2. слабая; 3. нельзя определить. |
17) Наиболее кислым следует считать раствор, в котором:
1. рН = 0 |
2. рН = 1 |
3. рН = 7 |
4. рН = 10 |
18) Гидролизу не подвергается соль: |
|
||
1. Na2CO3 |
2. Na2SO4 |
3. FeCl3 |
4. ZnCl2 |
19) Гидролизу в водном растворе подвергается соль:
1. NaCl 2. MgCO3 3. Na2SO4 4. КNO3
20) Наиболее щелочным следует считать раствор, в котором: 1. рН = 10 2. рН = 1 3. рН = 7 4. рН = 12
ТРУДНОРАСТВОРИМЫЕ ЭЛЕКТРОЛИТЫ
При растворении труднорастворимых электролитов в воде протекает реакция:

(тв) |
(р-р) |
Раствор, равновесный с твердой фазой растворенного вещества называют насыщенным. Концентрация вещества в насыщенном растворе характеризует его растворимость (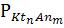 , моль/л). В справочных таблицах величину растворимости
, моль/л). В справочных таблицах величину растворимости
приводят в граммах растворенного вещества на 100г растворителя.
Константу равновесия реакции растворения труднорастворимого электролита называют произведением растворимости и обозначают символом 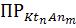 :
:
(12)
Правило произведения растворимости:
При данной температуре в насыщенном растворе труднорастворимого электролита произведение концентраций ионов, возведенных в степени, равные стехиометрическим коэффициентам, – величина постоянная, называемая произведением растворимости.
Оно справедливо, если единственными продуктами при растворении электролитов являются ионы, а меж-ионные и ионно-молекулярные взаимодействия ничтожно малы (система близка к идеальной).
Концентрация ионов в насыщенном растворе равна:
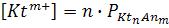 , моль/л
, моль/л
и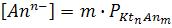 , моль/л , (13)
, моль/л , (13)
где:  – растворимость труднорастворимого электролита, моль/л.
– растворимость труднорастворимого электролита, моль/л.
Величина ПР – термодинамическая константа вещества, зависящая только от температуры, если раствор, находящийся в равновесии с осадком (насыщенный раствор), идеален.
ЛАБОРАТОРНАЯ РАБОТА № 2
ОПРЕДЕЛЕНИЕ рН НАЧАЛА ОСАЖДЕНИЯ ГИДРОКСИДОВ МЕТАЛЛОВ
Цель работы: определить величину рН начала осаждения гидроксида кобальта Со(ОН)2. По экспериментальным данным рассчитать 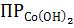 .
.
Значение рН при которых начинается выделение осадков малорастворимых гидроксидов металлов, называют рН гидратообразования. Зная эту величину, можно
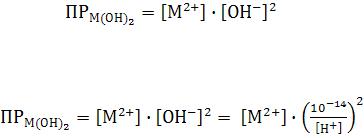
определить ПР М(ОН)2. Величина рН гидратообразования может быть рассчитана и определена экспериментально.
В растворе соли двухвалентного металла при достижении рН гидратообразования устанавливается равновесие:
М2+ + 2ОН- М(ОН)2(тв)
р-р
(14)
Зная, что в растворе  , получим
, получим
(15)
Величина рН гидратообразования зависит от концентрации соли. Она зависит так же от посторонних электролитов в растворе. По экспериментальной величине рН можно рассчитать значение 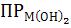 .
.
Экспериментальная часть.
Для измерения величины рН гидратообразования и величины произведения растворимости гидроксида кобальта используют потенциометрическое титрование его соли раствором щелочи. Измерительная ячейка состоит из стеклянного (индикаторного) электрода и хлоридсеребряного электрода (электрод сравнения), погруженных в исследуемый раствор; рН исследуемого раствора фиксируется с помощью иономера, шкала которого градуирована в единицах рН.
1.Включите иономер в сеть, промойте электроды многократно и тщательно дистиллированной водой, осторожно осушая каждый раз мембрану электродов фильтрованной бумагой.
2.В стакан поместите 50 мл 0,1 Н раствора соли кобальта и определите его рН.
3.Соберите установку для потенциометрического титрования: электрометрическую ячейку поместите на магнитную мешалку, опустите в раствор «магнитик» и над отверстием в держателе электродов установите бюретку, заполненную до нулевой отметки раствором щелочи (NaOH или KOH) известной концентрации (1Н и более). Включите мешалку.
4.Проведите титрование раствора. Чтобы получить более точные результаты, в начальный и конечный момент титрования добавляйте щелочь малыми порциями. Начинайте с одной капли, увеличивая объем щелочи до 0,1; 0,2; 0,3; 0,5мл. Затем – по 0,5мл и после резкого скачка рН – вновь добавляйте раствор щелочи по 0,1 мл. После каждого добавления новой порции раствора щелочи измеряйте рН исследуемого раствора. Результаты измерений занесите в таблицу:
V щелочи, мл
рН
5.На основании полученных данных постройте кривую титрования раствора соли кобальта раствором щелочи известной концентрации в координатах рН р-ра – V р-ра щелочи, мл.
6.Анализ кривой титрования.
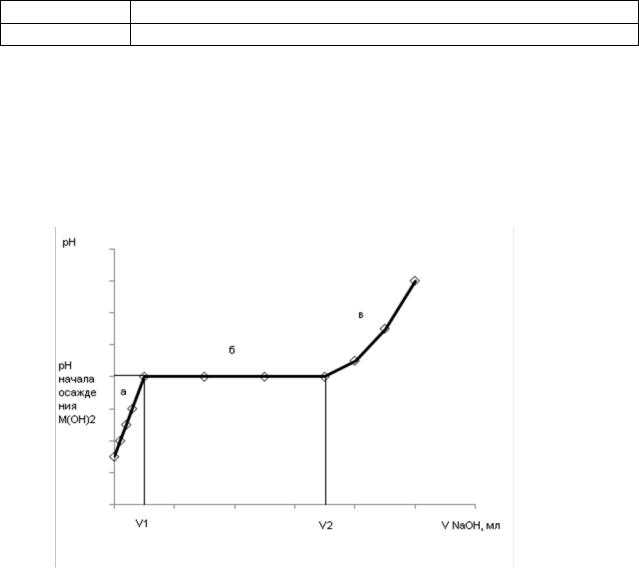
Примерный ход кривой титрования представлен на рис:
На участке «а» по мере добавления щелочи рН раствора возрастает до начала появления осадка гидроксида металла. Горизонтальная площадка кривой (участок «б») соответствует рН образования гидроксида (когда рН образования гироксида достигнут и выпадение осадка продолжается, добавление щелочи практически не изменяет величину рН раствора). Увеличение рН на участке «в» связано с накоплением в растворе (избыточной) свободной щелочи.
7. Расчет 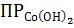 .
.
По найденной по графику величине рН образования гидроксида и соответствующей ему величине концентрации ионов водорода (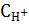 ), рассичайте
), рассичайте
концентрацию ионов ОН- (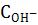 ) в растворе над осадком по формулам:
) в растворе над осадком по формулам:
 ,
,
 ,
,
Зная исходную концентрацию раствора соли кобальта (0,05 моль/л), а так же концентрацию щелочи (Сщелочи, моль/л) и объем щелочи, пошедший на осаждение Со(ОН)2, равный (V2-V1), рассчитайте число моль Со2+, связанных в осадок (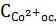 ):
):

; |
; |
; |
 ;
; 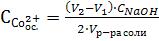 .
.
Причем Vр-ра соли = 50 мл.
Равновесную молярную концентрацию ионов Со2+ (моль/л) определите как разность между исходной концентрацией Со2+ и концентрацией ионовСо2+, вступивших в реакцию:
Со2+ + 2 ОН- Со(ОН)2(тв)
Тогда равновесная концентрация ионов Со2+ равна:
;
Величина
Сравните полученную величину ПР с табличными данными.
Сделайте выводы по проделанной работе.
ТЕСТ 2
Труднорастворимые электролиты.
1)Электролиты – это вещества . . .
2)Труднорастворимые электролиты – это . . .
3)Константа равновесия реакции растворения труднорастворимого электролита называется . . .
4)В насыщенном растворе труднорастворимого электролита произведение концентраций ионов есть величина . . . , называемая . . .
5)Для труднорастворимого электролита KtnAnm правило произведения растворимости представлено выражением:
1. 
2. 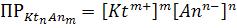
3. 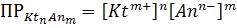
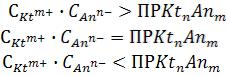
6) Величина ПР зависит от:
1.температуры, природы растворенного вещества, его концентрации;
2.температуры, природы растворенного вещества, природы растворителя;
3.температуры, природы растворенного вещества, природы растворителя, концентрации;
7)Растворимость вещества (Р) – это . . .
8)Величину молярной растворимости рассчитывают по величине произведения растворимости по формуле:
1. 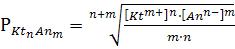 ;
;
2. 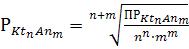 ;
;
3. 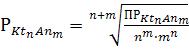 .
.
9) В насыщенном растворе над осадком Мg(ОН)2 концентрация ионов Мg2+:
1)Равна растворимости [Mg2+] = P(Мg(ОН)2);
2)Больше P(Мg(ОН)2 в 2 раза;
3)Меньше P(Мg(ОН)2 в 2 раза.
10)Если ПР (Мg(ОН)2) =6∙10-10, то растворимость его P(Мg(ОН)2) равна:
1)5,3∙10-4 моль/л;
2)1,73∙10-5 моль/л;
3)5,5∙10-4 моль/л;
11)Установите соответствие:
Раствор |
Соотношение |
|
1. |
Насыщенный |
А. |
2. |
Ненасыщенный |
Б. |
3. |
Пересыщенный |
В. |
|
|
|
Условием выпадения осадка является: 1. А
2. Б
