
5900
.pdfМинистерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего
профессионального образования
«Нижегородский государственный архитектурно-строительный университет»
Я.А. Васина, И.Л. Смельцова
ХИМИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО АНАЛИЗА
Учебно-методическое пособие к выполнению лабораторных работ по химии для студентов ННГАСУ направления 05.03.06 Экология и Природопользование, направленность (профиль) Природопользование
Нижний Новгород, 2016
2
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего
профессионального образования
«Нижегородский государственный архитектурно-строительный университет»
Я.А. Васина, И.Л. Смельцова
ХИМИЧЕСКИЕ МЕТОДЫ КОЛИЧЕСТВЕННОГО АНАЛИЗА
Учебно-методическое пособие к выполнению лабораторных работ по химии для студентов ННГАСУ направления 05.03.06 Экология и Природопользование, направленность (профиль) Природопользование
Нижний Новгород, 2016
3
УДК 543.061
Васина Я. А., Смельцова И.Л. Химические методы количественного анализа. [Электронный ресурс]: учебно-метод. пос./ Я.А. Васина, И.Л. Смельцова; Нижегор. гос. архитектур.-строит. ун-т -Н.Новгород: Издание ННГАСУ, 2016. – 49 с, ил. 1.электрон. опт. диск (CD-R)
В методических указаниях описываются основные этапы количественного анализа веществ, излагается сущность гравиметрического и титриметрического методов анализа, приводятся методики определения ряда веществ в объектах окружающей среды, примеры расчетов, выполняемых по результатам анализа.
Учебно-методическое пособие к выполнению лабораторных работ по химии для студентов ННГАСУ направления 05.03.06 Экология и Природопользование, направленность (профиль) Природопользование
Составители: доц. Я.А. Васина доц. И.Л. Смельцова
Под редакцией проф. В.А. Яблокова
© Нижегородский государственный архитектурно-строительный университет, 20016.
4
ТЕРМИНЫ, ОПРЕДЕЛЕНИЯ И ОБОЗНАЧЕНИЯ МЕТРОЛОГИЧЕСКИХ ХАРАКТЕРИСТИК АНАЛИЗА ВЕЩЕСТВ
Термины |
Определения |
Обозначения, |
|
|
примечания |
1 |
2 |
3 |
1.Анализ вещества |
Получение опытным путем |
Термин |
|
данных о химическом |
распространяется на |
|
составе вещества |
любые методы анализа |
|
|
вещества |
2. Метод анализа |
Краткое описание |
Примеры: |
вещества |
принципов, положенных в |
титриметрический |
|
основу анализа вещества |
анализ, |
|
|
фотометрический анализ |
|
|
и др. |
3.Количественный |
Экспериментальное |
В дальнейшем |
анализ вещества |
определение (измерение |
выражение |
|
концентрации, количества) |
«концентрация» |
|
химических элементов |
заменяется словами |
|
соединений или их форм в |
«содержание |
|
анализируемом веществе, |
определяемых |
|
выраженное в виде числа с |
компонентов» или |
|
указанием стандартного |
«определяемое |
|
отклонения |
содержание» |
4.Методика |
Подробное описание всех |
В описании методики |
анализа |
условий и операций, |
указывают, например, |
|
которые обеспечивают |
анализируемый |
|
регламентированные |
материал, условия |
|
характеристики |
пробоотбора, средства |
|
воспроизводимости и |
измерений, диапазон |
|
правильности |
определяемых |
|
|
содержаний, способ |
|
|
получения |
|
|
градуировочной |
|
|
характеристики, число |
|
|
параллельных |
|
|
определений, |
|
|
продолжительность |
|
|
анализа, характеристики |
|
|
правильности и |
|
|
воспроизводимости |
5
1 |
2 |
3 |
5. Проба |
Часть анализируемого |
а. В отдельных случаях в |
|
материала, |
качестве пробы |
|
представительно |
используют весь |
|
отражающая его |
анализируемый |
|
химический состав |
материал |
|
|
б. В зависимости от |
|
|
решаемой задачи проба |
|
|
должна отражать |
|
|
средний состав всего |
|
|
анализируемого |
|
|
материала или |
|
|
определенной его части |
|
|
(фазы, слоя, и т. п.) |
6. Аналитичеcкая |
Определенная часть пробы, |
В отдельных случаях в |
навеска |
используемая при |
качестве аналитической |
|
выполнении единичного |
навески используют всю |
|
определения |
пробу |
7. Аналитический |
Среднее математическое |
а. Обозначение: у |
сигнал |
ожидание результатов |
б. Примеры: оптическая |
|
измерения физической |
плотность в фотометрии, |
|
величины в |
площадь пика в газовой |
|
заключительной стадии |
хроматографии и т.п. |
|
анализа, функционально |
|
|
связанной с содержанием |
|
|
определяемого компонента |
|
8. Градуировочная |
Зависимость |
Градуровочный график |
характеристика |
аналитического сигнала от |
может представлять |
|
содержания определяемого |
собой зависимость |
|
компонента, установленная |
преобразованной |
|
опытным путём или |
величины |
|
расчетом и выраженная в |
аналитического сигнала |
|
виде формул |
от определяемого |
|
(градуировочная функция), |
содержания |
|
таблиц или графиков |
|
9. Предел |
Наименьшее содержание, |
а. Обозначение: Сmin,р, |
обнаружения |
при котором по данной |
где р- доверительная |
|
методике можно |
вероятность |
|
обнаружить присутствие |
б. Сmin,р находят при |
|
определяемого компонента |
помощи градуировочной |
|
с заданной доверительной |
характеристики по |
|
вероятностью |
величине минимально |
|
|
обнаруживаемого |
|
|
сигнала |
6
1 |
2 |
3 |
10. Единичное |
Однократное проведение |
Термин «наблюдение» |
определение |
всей последовательности |
по смыслу совпадает с |
|
операций, |
термином «единичное |
|
предусмотренных |
определение» |
|
методикой анализа |
|
11. Результат |
Значение содержания |
а. Обозначения: С - |
единичного |
определяемого |
концентрация; q – |
определения |
компонента, найденное при |
количество вещества |
|
единичном определении |
б. Наряду со значениями |
|
|
определяемых |
|
|
содержаний следует |
|
|
приводить единицы их |
|
|
измерения |
12. Параллельные |
Получения нескольких |
Интервал времени, в |
определения |
результатов единичных |
течение которого, |
|
определений для одной |
выполняются |
|
пробы практически в |
параллельные |
|
одинаковых условиях при |
определения, соизмерим |
|
фиксированной |
с длительностью |
|
градуировочной |
единичного определения |
|
характеристике |
|
13.Результат |
Среднее значение |
Наряду с результатом |
анализа |
результатов параллельных |
анализа должен |
|
определений |
приводиться |
|
|
доверительный интервал |
1. АНАЛИТИЧЕСКАЯ СЛУЖБА И ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС
Информация о составе вещества – необходимое условие успешного управления любым технологическим процессом, обеспечения надлежащего качества сырья и продукции, решения экологических проблем.
Аналитическую службу можно определить как сложную систему, действующую с целью получения данных о химическом составе, реже – химическом строении веществ, которые необходимы для материального производства, рационального использования природных ресурсов и охраны среды, здравоохранения, научных исследований.
Цели анализа, конкретные задачи перед аналитической службой в целом и аналитиком ставит сама жизнь, уровень развития производства, культуры. Далее в деятельности аналитиков возникает необходимость в выборе методов анализа конкретного объекта. В рамках выбранного метода разрабатываются методики анализа.

7
Разработкой теоретических основ методов анализа и созданием методик анализа занимаются аналитики научно – исследовательских институтов и лабораторий, крупнейших заводских лабораторий, кафедр аналитической химии вузов. В контрольных лабораториях предприятий, имея информацию о существующих методах и методиках анализа, выбирают наиболее подходящие в каждом конкретном случае.
Полученные результаты анализа обрабатываются. На основе этих данных делается вывод о химическом составе исследуемого объекта.
СТРУКТУРНАЯ СХЕМА ПРОИЗВОДСТВА ВЕЩЕСТВА (ПРОДУКТА, МАТЕРИАЛА) И ЕГО КОНТРОЛЬ.
Блок управляющих решений с учетом данных о химическом составе
Данные о химическом составе
|
|
|
|
Химический |
Химический |
|
Аналитический |
|
|
анализ |
|
контроль |
|
анализ |
|
|
|
|
|
|
|
|
|
|
Сырье |
|
|
|
Продукция |
|
Технологический |
|
||
|
|
процесс |
|
|
|
|
|
|
|
|
|
|
|
|

8
СХЕМА ДЕЯТЕЛЬНОСТИ АНАЛИТИКА
Постановка целей и задач |
|
Выбор |
|
Выполнение |
анализа объекта на |
|
метода |
|
анализа |
содержание компонентов |
|
анализа |
|
|
|
|
|
|
|
Характеристика |
|
Интерпретация |
|
Результаты |
анализируемого |
|
результатов |
|
анализа |
объекта |
|
анализа |
|
|
|
|
|
|
|
Вопросы
1.Какой этап в деятельности аналитика вы считаете наиболее ответственным?
2.На каких этапах в этой деятельности может включиться специалист по охране окружающей среды?
3.Какие знания ему для этого необходимы?
Аналитики должны уметь надежно, по возможности быстро, определять содержание различных компонентов в атмосфере, поверхностных, подземных водах, сточных водах предприятий и коммунальных служб, в почве; осуществлять контроль за качеством выпускаемой продукции.
2.ПРИНЦИПЫ ХИМИЧЕСКИХ МЕТОДОВ АНАЛИЗА
Химический анализ традиционно делят на качественный и количественный. Если знание принципов и техники эксперимента качественного анализа позволяет ответить на вопрос: какие компоненты содержатся в анализируемом объекте, то цель количественного анализа – установить их содержание или концентрацию.
В химическом качественном анализе идентификация веществ достигается путем выполнения аналитических реакций.
Аналитическая реакция сопровождается возникновением сигнала (аналитического сигнала), фиксируемого визуально или приборами. Число визуальных сигналов невелико: появление новой фазы (реакции осаждения или идущие с выделением газа), изменение окраски (цветные реакции).
Вопросы
1.Какие реакции называют аналитическими?
2.Сформулируйте основные критерии выбора аналитических реакций?

9
3. Дайте определения понятий: предел обнаружения, предельное отношение, специфический реагент.
Вхимических методах количественного анализа также используют аналитическую реакцию определяемого компонента (Х) с выбранным реактивом (R): Х + R = Р. Реакции, как правило, проводят в растворах.
Методы количественного анализа можно разделить на химические (классические), физико-химические и физические (инструментальные).
Взависимости от типа реакции и способа её проведения выделяют два химических метода количественного анализа: весовой анализ (гравиметрия)
иобъёмный анализ (титриметрия).
Вгравиметрическом анализе определяемое вещество (Х) отделяют от других компонентов анализируемого объекта осаждением подходящим реактивом (R) в виде чистого соединения известного состава XaRb: aX + bR =
↓XaRb.
Осадок отделяют от раствора фильтрованием, промывают, просушивают, прокаливают при определённой температуре, чтобы получить в виде чистого соединения определенного состава. Массу осадка определяют взвешиванием на аналитических весах с точностью до 0,0004 г. По массе осадка m(XaRb) рассчитывают массу mx определяемого компонента и его концентрацию в анализируемом объекте:
mx = mХa Rb × M X × a , где
M X a Rb
mx – масса определяемого компонента, г;
mX a Rb – масса взвешиваемого осадка (весовой формы),г;
Mx – молярная масса определяемого компонента Х, г/моль; M X a Rb – молярная масса осадка, г/моль;
а – число атомов определяемого компонента в молекуле осадка XaRb.
Отношение M X × a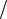 M X a Rb называют фактором пересчета с массы весовой формы осадка на массу определяемого компонента (аналитический
M X a Rb называют фактором пересчета с массы весовой формы осадка на массу определяемого компонента (аналитический
множитель). Если его |
обозначить, |
|
как F = |
a × M x |
, то формула расчета |
|
|
|
|||||
|
|
|
|
|
M X R |
|
|
|
|
|
|
a b |
|
примет вид: |
mx |
= mX |
R |
× F |
||
|
|
a b |
||||
В объёмном анализе концентрацию определяемого компонента (Х) в растворе рассчитывают по объёму раствора реактива (R) с точно известной концентрацией, пошедшему на взаимодействие с измеренным объёмом раствора определяемого компонента. Для этого к раствору определяемого компонента постепенно небольшими порциями добавляют раствор реактива. Этот процесс называют титрованием. Раствор реактива с точно извествной концентрацией называют титрантом или рабочим раствором.. После

10
добавления каждой порции титранта в растворе устанавливается равновесие реакции титрования:
Хр-р + Rр-р = Р, где Р – продукты реакции.
Реакция, используемая при титровании, должна отвечать следующим требованиям: 1)быть строго стехиометричной и воспроизводимой; 2)протекать быстро; 3)протекать количественно, т.е. константа равновесия реакции должна быть достаточно высокой; 4)должен существовать способ фиксации точки эквивалентности.
Точкой эквивалентности в процессе титрования называют момент титрования, когда определяемый компонент и реагент прореагируют равным числом эквивалентов (стехиометрично):
|
|
|
m X |
= |
mR |
|
(закон эквивалентов) |
|
|
|
Э Х |
ЭR |
|||
|
|
|
|
|
|||
В объёмном анализе закон эквивалентов удобнее записать в другой |
|||||||
форме: |
|
|
|
|
|
|
|
|
|
H X ×VX = H R ×VR |
или H X ×VX = HT ×VT , где |
||||
Vx - объём исследуемого раствора, взятый на анализ, мл. |
|||||||
VR или VТ – |
объём раствора реактива с точно известной концентрацией |
||||||
(титранта). |
|
|
|
|
|
|
|
Нх – |
нормальность исследуемого раствора, экв/л. |
||||||
НR |
или НТ – |
нормальность титранта, экв/л. |
|||||
Тогда H X = VT × HT
VX
На основе этой формулы можно выразить концентрацию определяемого компонента в других единицах:
Х,г / л = VT × H T × ЭX
VX
Х, мг / л = VT × H T × ЭX ×1000 , где
VX
Эх – эквивалентная масса определяемого вещества (в терминологии ЮПАК - молярная масса эквивалента).
Конец титрования устанавливают по изменению окраски индикатора. Индикаторы – вещества, которые изменяют свою окраску или какое – либо другое свойство (например, агрегатное состояние, цвет или интенсивность флуоресценции) в точке эквивалентности или вблизи неё. Индикаторы добавляют перед началом титрования в титруемый (анализируемый) раствор.
Экспериментально титрование прекращают, когда индикатор изменит свою окраску или другое свойство. Этот момент называют конечной точкой титрования (КТТ). Чаще всего она не совпадает с теоретически рассчитанной точкой эквивалентности. Индикатор выбирают так, чтобы точка конца
