
книги / Процессы тепломассопереноса в гетерогенных системах
..pdf
Ц N1
|
N |
|
|
|
|
L u k i |
2 |
|
|
|
|
D |
k i |
0,5 |
exp |
|
. |
(61) |
|
|
|
|
|||||||
|
эф |
|
|
|
Dэф k i |
|
|
||
|
i 1 |
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
Здесь k – длина единичного импульса, k TN (T – длина
полного импульса ввода индикатора, с); N – выбранное число деления импульса; L – длина реактора; δ – вспомогательное число, например 1·10–6.
Понятно, что одним из условий такого решения является неявное предположение о том, что свойства среды практически не меняются при растворении в ней выбранного индикатора.
В этом случае отклик реактора на внешнее возмущение на входе выражается функцией от времени Ц(τ) (61).
4.3. Пример определения критерия Пекле
На рис. 15 приведён пример определения критерия Пекле по экспериментальным данным. В столбце θ приведены значения времени замера концентрации индикатора на выходе из реактора от момента ввода пробы. Концентрации индикатора приведены в столбце «CEXP».
На этом рисунке использованы следующие обозначения: L – характерная длина реактора, м; w – скорость движения сырья вдоль реактора, м/с; T – фактическая длительность импульса ввода индикатора, с; k – выбранная для расчёта длина единичного импульса, с; Def – коэффициент продольной диффузии, м2/с, который подбирается таким образом, чтобы теоретическая кривая максимально точно совпала с экспериментальными значениями концентрации; ω – вспомогательное число.
Длина импульса меньше среднего времени прохождения через реактор.
51

Рис. 15. Пример определения критерия Пекле
52

На рис. 16 приведён пример неудачной аппроксимации, поскольку выбранный Def = 1 м2/с не соответствует реальному значению.
Рис. 16. Пример неудачной аппроксимации при определении критерия Пекле
Основными задачами при выполнении практической работы по разделу 4 являются:
1.Ознакомление с диффузионно-кинетической моделью процесса.
2.Исследование влияния различных параметров процесса на его результаты.
3.Приобретение навыка математической обработки экспериментальных данных с помощью приведённой математической модели процесса.
Задания при изучении модели:
1.На основании физико-химических знаний описать влияние каждого из факторов приведённой модели на вид кривой отклика химического реактора на сложное возмущение.
2.Объяснить идеологию построения математической мо-
дели.
53
3.Объяснить назначение каждого члена уравнения, описывающего кривую отклика реактора на внешнее возмущение.
4.Объяснить принцип поиска неизвестных параметров на основании экспериментальных данных.
5.Пояснить причину изменения вида зависимостей при изменении входных кинетических и диффузионных параметров модельного уравнения.
6.Используя метод минимизации отклонений, определить неизвестные параметры модели по экспериментальным данным.
7.Расширить предложенную модель на случай протекания в системе химической реакции первого порядка.
54
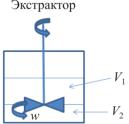
5. МЕЖФАЗНЫЙ ПЕРЕНОС, СОПРЯЖЁННЫЙ С ХИМИЧЕСКОЙ РЕАКЦИЕЙ В ЭКСТРАКЦИОННОЙ СИСТЕМЕ
Щелочная очистка лёгкой бензиновой фракции (гексана) от меркаптанов (рис. 17) протекает по следующим реакциям:
RSH NaOH k1 RSNa H2O;
RSH NaOH RSNa H O.
k2 2
Константа равновесия реакции |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Kp может быть записана следую- |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
щим выражением: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
RSNa H2O |
|
|
|
|
|
Рис. 17. Экстрактор (реактор |
|||||||||||
K |
|
|
. |
(62) |
|
|
|
|
с мешалкой) для щелочной |
||||||||||||
p |
RSH NaOH |
|
|
|
|
||||||||||||||||
|
|
|
|
|
очисткигексанаотмеркаптанов |
||||||||||||||||
Математическая модель щелочной очистки гексана имеет |
|||||||||||||||||||||
вид: |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dС |
0 V2 |
S C0 C1 ; |
|
|
|||||||||||||
|
|
|
|
dt |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
k1 |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
dC1 |
V2 S C0 C1 V1 |
k1C1C2 |
C3 ; |
|||||||||||||||||
|
|
||||||||||||||||||||
|
|
dt |
|
|
|
|
|
|
V |
|
|
|
|
K |
p |
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
(63) |
|||
|
|
|
|
dC2 |
|
|
|
|
|
|
k1 |
|
|
|
|||||||
|
|
|
|
k1C1C2 |
|
|
C3 ; |
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
dt |
|
|
|
|
|
|
Kp |
|
|
|
|
|
|||
|
|
|
|
|
|
dC3 |
|
|
|
|
|
k1 |
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
k1C1C2 |
|
|
C3 , |
|
|
|||||||||
|
|
|
|
|
|
dt |
|
|
Kp |
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
где k1 – константа скорости прямой реакции; Kp – константа равновесия реакции; S – удельная поверхность эмульсии, м2/м3; V1 и V2 – исходный объём гексана с растворённым бутилили амилмеркаптаном и водного раствора щёлочи соответственно, м3;
55
C0 – концентрация меркапатана в гексане, кмоль/м3; C1 – концентрация меркаптана в воде, кмоль/м3; C2 – концентрация щёлочи в воде, кмоль/м3; C3 – концентрация меркаптида натрия в воде, кмоль/м3; β – коэффициент массопереноса; t – длительность протекания химической реакции, мин; φ – коэффициент распределения меркаптана между углеводородом и водой.
Математическая модель щелочной очистки предусматривает несколько стадий процесса, включая массоперенос меркаптанов из углеводородной фазы в водный щелочной раствор через поверхность раздела фаз, что описывается первым уравнением системы (63). Движущей силой процесса массопереноса является разность активностей меркаптана в этих фазах. В первом приближении можно принять, что активности равны мольным концентрациям меркаптана в соответствующих фазах с учётом термодинамического коэффициента распределения его между ними (φ) [13]. Три последующих уравнения системы (63) описывают межфазный материальный баланс и кинетику прямой и обратной реакций в водном растворе.
Равновесный диаметр капли при перемешивании углеводорода с водной фазой по Колмогорову [4] определяется соотношением:
|
3 |
2 |
|
, |
(64) |
dк A |
3 |
D6м |
|
||
|
|
w |
|
|
|
где А – коэффициент пропорциональности; σ – межфазная энергия на границе между водной и углеводородной фазами; Dм – диаметр перемешивающего устройства (мешалки); ρ – плотность эмульсии; w – линейная скорость движения потока сырья внутри аппарата.
Простые преобразования позволяют на основании (64) вывести уравнение для поверхности эмульсии F(Re), или F(w), образующейся при перемешивании несмешивающихся фаз в моно-
56

дисперсном приближении. На рис. 18 представлена математическая модель процесса извлечения меркаптанов из бензиновой фракции за счёт реакции с водным раствором щёлочи.
Рис. 18. Математическая модель процесса извлечения меркаптанов из бензиновой фракции в Mathcad
(пример расчёта каталитического процесса) (см. также с. 58)
57

Рис. 18. Окончание
58
Основными задачами при выполнении практической работы по разделу 5 являются:
1.Ознакомление с технологией и основными физикохимическими параметрами, влияющими на протекание процесса межфазного взаимодействия меркаптанов, содержащихся в бензиновой фракции, и водного раствора NaOH.
2.Ознакомление с диффузионно-кинетической моделью процесса.
3.Исследование влияния различных параметров процесса на его результаты.
4.Приобретение навыка математической обработки экспериментальных данных с помощью приведённой математической модели процесса.
Задания при изучении модели:
1.На основании физико-химических знаний описать влияние каждого из факторов приведённой модели на скорость и результаты очистки.
2.Объяснитьидеологиюпостроенияматематическоймодели.
3.Объяснить назначение каждого уравнения математической модели.
4.Объяснить необходимость применения процедуры «rkadapt» вместопроцедуры«rkfixed».
5.Пояснить значения начальных условий при решении матрицы уравнений.
6.Объяснить принцип поиска неизвестных параметров на основании экспериментальных данных и приведённой точной модели процесса.
7.Пояснить причину изменения вида зависимостей при изменениивходныхкинетическихидиффузионныхпараметровмодели.
8.Используя МНК, определить неизвестные параметры модели по экспериментальным данным.
59
6.ИСПАРЕНИЕ ВЕЩЕСТВ
6.1.Теория процесса испарения
Процессы испарения жидкости или возгонки твёрдого тела имеют большое значение в различных технологических операциях и часто являются лимитирующей стадией, определяющей скорость их протекания. Самостоятельное значение эти процессы имеют в технологиях парового нанесения покрытий при выращивании сложных многослойных компонентов электронных схем или защитных покрытий. Они имеют ряд преимуществ перед традиционными методами нанесения покрытий и в последнее время развиваются достаточно интенсивно.
Следует заметить, что процесс испарения с поверхности веществ происходит всегда, но его интенсивность связана со многими факторами.
Следует различать равновесное состояние и динамический процесс, определяемые термодинамическими и, соответственно, кинетическими факторами.
Испарение – эндотермический процесс, при котором поглощается теплота фазового перехода, которая затрачивается на преодоление сил молекулярного сцепления и на работу расширения из-за превращениячастиконденсированноготелавпарбольшогообъёма.
Если поместить тело в вакуум в замкнутом объёме, то за счёт испарения над ним соберётся определённое равновесное количество пара этого вещества и установится так называемое давление насыщенных паров (ДНП), величина которого индивидуальна для каждого вещества. Величина ДНП зависит от ряда термодинамических параметровиописываетсяуравнениемКлапейрона– Клаузиуса[13]:
dp |
|
Q |
, |
(65) |
dT |
T Vп Vж |
|||
где p – давление насыщенного пара; Q – |
теплота испарения; |
|||
Vп, Vж – молярные объёмы пара и жидкости; Т – температура.
60
