
М ИНИСТЕРСТВО
НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ
ФЕДЕРАЦИИ
ИНИСТЕРСТВО
НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ
ФЕДЕРАЦИИ
федеральное государственное бюджетное образовательное учреждение
высшего образования
«Тольяттинский государственный университет»
(наименование института полностью)
Кафедра /департамент /центр1 институт химии и энергетики
(наименование кафедры/департамента/центра полностью)
13.03.02 Электроэнергетика и электротехника
(код и наименование направления подготовки, специальности)
(направленность (профиль) / специализация)
лабораторная работа №__3_
по учебному курсу «_Физика 1__________»
(наименование учебного курса)
Вариант __4__ (при наличии)
Студент |
Яшин И.А. (И.О. Фамилия) |
|
Группа |
ЭЭТбп-1801а (И.О. Фамилия) |
|
Преподаватель |
Леванова Наталья Геннадьевна (И.О. Фамилия) |
|
Тольятти 2021
«Теплоемкость идеального газа»
Цель работы:
Знакомство с теплоемкостью идеального газа в изохорическом и изобарическом процессах.
Экспериментальное подтверждение закономерностей изопроцессов.
Экспериментальное определение количества степеней свободы и структуры молекул газа в данной модели.
Результаты измерений и расчетов:
1.
Одноатомный
газ: V0=70
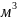 ,
p0=200
Па, ν=1,8 кмоль
,
p0=200
Па, ν=1,8 кмоль
Таблица 2
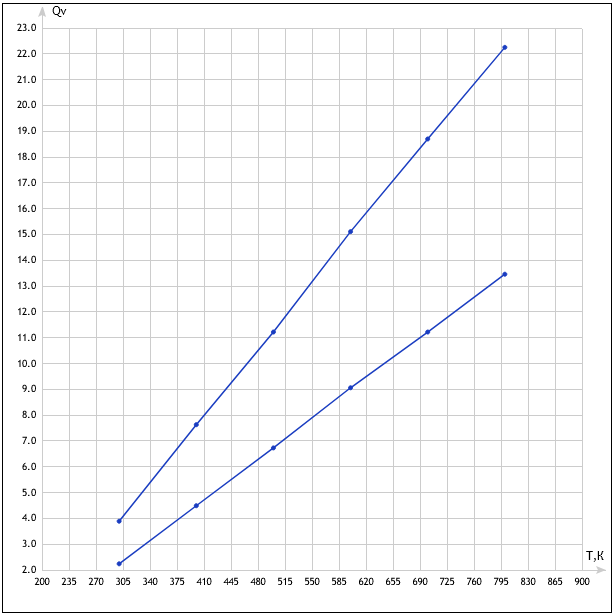
Т, К |
300* |
400 |
500 |
600 |
700 |
800 |
QV, кДж |
2,24 |
4,49 |
6,73 |
9,06 |
11,22 |
13,46 |
Qр, кДж |
3,89 |
7,63 |
11,22 |
15,11 |
18,7 |
22,25 |
*Значения абсолютной температуры может не совпадать с рекомендуемым, но должно быть близким по значению и одинаковым для Qp и QV в столбце.
График 1 зависимость температуры от кол-ва теплоты (одноатомный газ).
Определение Cp теплоемкости и cp молярной теплоемкости газа при постоянном давлении:
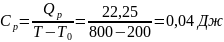
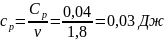
Определение CV теплоемкости и cV молярной теплоемкости газа при постоянном объеме:
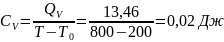
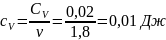
Определение
γ
постоянной адиабаты:
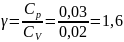
Определение i числа степеней свободы молекул газов:
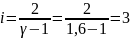
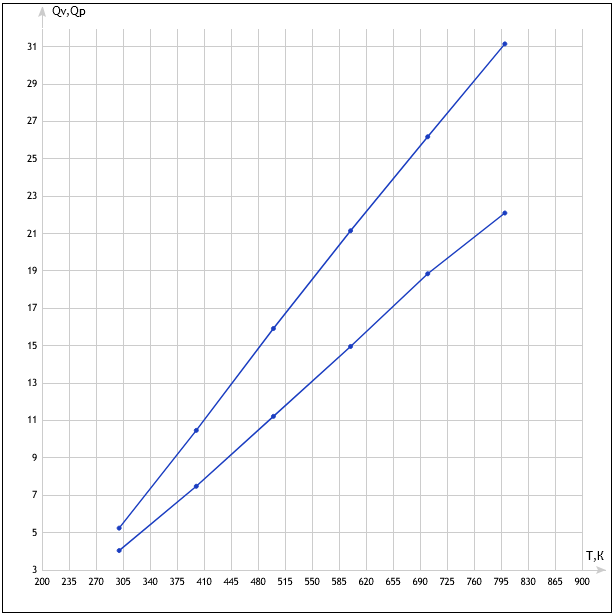
2. Двухатомный газ: V0=70 , p0=200 Па, ν=1,8 кмоль
Таблица 3
Т, К |
300 |
400 |
500 |
600 |
700 |
800 |
QV, кДж |
4,04 |
7,48 |
11,22 |
14,96 |
18,85 |
22,1 |
Qр, кДж |
5,24 |
10,47 |
15,92 |
21,15 |
26,18 |
31,15 |
График 2 зависимость температуры от кол-ва теплоты (двухатомный газ).
Определение Cp теплоемкости и cp молярной теплоемкости двухатомного газа при постоянном давлении:
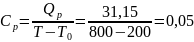
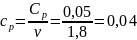
Определение CV теплоемкости и cV молярной теплоемкости двухатомного газа при постоянном объеме:
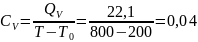
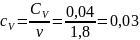
Определение
γ
постоянной адиабаты:
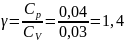
Определение i числа степеней свободы молекул газов:
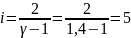
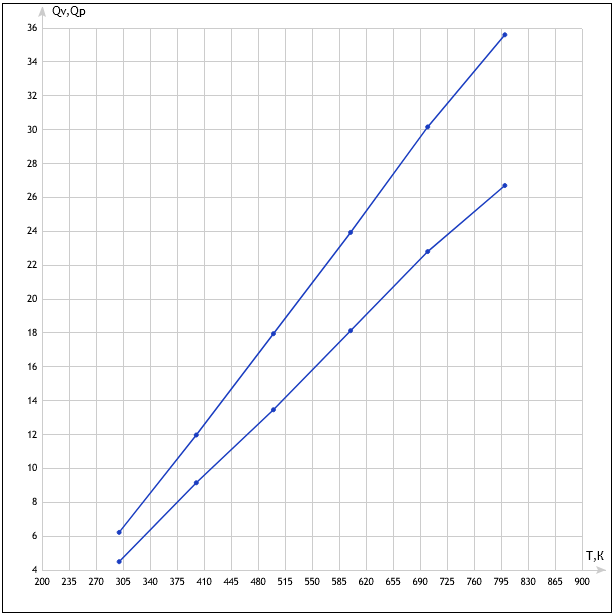
3. Трехатомный газ: V0=70 , p0=200 Па, ν=1,8 кмоль
Таблица 4
Т, К |
300 |
400 |
500 |
600 |
700 |
800 |
QV, кДж |
4,49 |
9,15 |
13,46 |
18,13 |
22,8 |
26,7 |
Qр, кДж |
6,22 |
11,97 |
17,95 |
23,93 |
30,16 |
35,6 |
График 3 зависимость температуры от кол-ва теплоты (трёхатомный газ).
Определение Cp теплоемкости и cp молярной теплоемкости трехатомного газа при постоянном давлении:
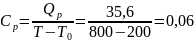
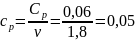
Определение CV теплоемкости и cV молярной теплоемкости трехатомного газа при постоянном объеме:
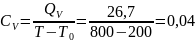
Определение
γ
постоянной адиабаты:
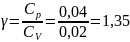
Определение i числа степеней свободы молекул газов:
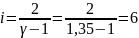
Вывод: чем больше степеней свободы у газа,тем большее кол-во энергии нужно сообщить газу,для увеличения его температуры.
1 Оставить нужное
