Задачи Крюкова / ЭДС 2
.docx1. Запишите уравнение химической реакции, протекающей самопроизвольно в элементе:
Ag | Pb | PbJ2 (тв) | KJ (р-р) | AgJ (тв) | Ag
Решение:
Левый
электрод: PbJ2
+ 2ē = Pb
+ 2J-
E
Правый
электрод: AgJ
+ ē = Ag
+ J-
E
= -0,152
Реакцию
левого электрода запишем в виде
окисления, а реакцию правого электрода
умножим на 2. Получим:
Левый
электрод: Pb
+ 2J-
= PbJ2
+ 2ē
Правый
электрод: 2AgJ
+ 2ē = 2Ag
+ 2J-
Сложим
реакции для получения общего уравнения
химической реакции.
2AgJ
+ Pb
= PbJ2
+ 2Ag
Дано: Т = 298К Е = 0,21069В Найти: ΔrG
,
ΔrН
,
и ΔrS


 = -0,365
= -0,365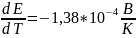

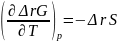
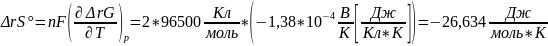
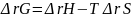
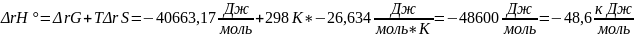
Ответ:
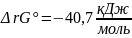 ,
,
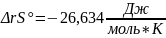 ,
,
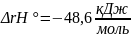
2. ЭДС гальванического элемента, составленного из насыщенного каломельного электрода (электрода сравнения) и хингидронного электрода (индикаторного) в данном растворе, рН которого неизвестен, при 298 К равна 0.163 В. Пользуясь справочными данными рассчитайте рН данного раствора, если электрод сравнения в данной цепи – отрицательный.
Дано: Каломельный
электрод (насыщенный) Хингидронный
электрод Е
= 0,163В Т
= 298К Найти: рН
1) Каломельный электрод – левый.
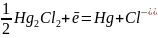
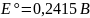
2) Хингидронный электрод – правый.

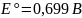
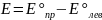
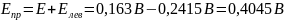
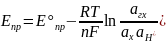 ;
n
= 2;
;
n
= 2;


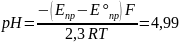
Ответ:
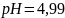
3. Пользуясь справочными данными рассчитайте константу равновесия реакции:
Sn2+ + ClO4– + H2O = Sn4+ + ClO3– + 2OH–
Дано: T
= 298К Найти:

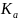
Решение:
Левый
электрод:

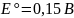
Правый
электрод:
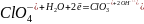
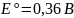
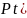

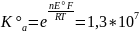
Ответ: