
3825
.pdf
И.М. Винокурова
ТОПЛИВА И РАБОЧИЕ ПРОЦЕССЫ В АВИАЦИОННЫХ И РАКЕТНЫХ ДВИГАТЕЛЯХ: СБОРНИК ПРАКТИЧЕСКИХ ЗАДАЧ
И УПРАЖНЕНИЙ
Учебное пособие
Воронеж 2014
ФГБОУ ВПО “Воронежский государственный технический университет”
И.М. Винокурова
ТОПЛИВА И РАБОЧИЕ ПРОЦЕССЫ В АВИАЦИОННЫХ И РАКЕТНЫХ
ДВИГАТЕЛЯХ: СБОРНИК ПРАКТИЧЕСКИХ ЗАДАЧ И УПРАЖНЕНИЙ
Утверждено Редакционно-издательским советом университета в качестве учебного пособия
Воронеж 2014
УДК 54
Винокурова И.М. Топлива и рабочие процессы в авиационных и ракетных двигателях: сборник практических задач и упражнений: учеб. пособие [Электронный ресурс]. – Электрон. текстовые и граф. данные (21,5 Мб) / И.М. Винокурова. – Воронеж: ФГБОУ ВПО “Воронежский государственный технический университет”, 2014. – 1 электрон. опт. диск (CD-ROM) : цв. – Систем. требования: ПК 500 и выше; 256 Мб ОЗУ; Windows XP; SVGA с разрешением 1024x768; Adobe Acrobat; CD-ROM диско-
вод; мышь. – Загл. с экрана.
Учебное пособие предназначено для оказания методической помощи студентам при выполнении практических работ по курсу “Топлива и рабочие процессы в авиационных и ракетных двигателях” с целью полного освоения материала и успешного выполнения заданий.
Издание соответствует требованиям Федерального государственного образовательного стандарта высшего профессионального образования по специальности 160700.65 “Проектирование авиационных и ракетных двигателей”, дисциплине “Топлива и рабочие процессы в авиационных и ракетных двигателях”.
Табл. 8. Ил. 22. Библиогр.: 10 назв.
Рецензенты: кафедра физики и химии Воронежского государственного архитектурно-строительного университета (зав. кафедрой д-р хим. наук, проф. О.Б. Рудаков); д-р техн. наук, проф. И.А. Чечета
Винокурова И.М., 2014
Оформление. ФГБОУ ВПО “Воронежский государственный технический университет”, 2014
ВВЕДЕНИЕ
Внимательного изучения материалов учебного пособия достаточно для формирования грамотных ответов при выполнении контрольных работ и сдачи зачета или экзамена по дисциплине “Топлива и рабочие процессы в авиационных и ракетных двигателях”.
Изучение любого вопроса на уровне сущности, а не на уровне отдельных явлений способствует более глубокому и прочному усвоению материала. Чтобы лучше запомнить и усвоить изучаемый материал, надо обязательно иметь рабочую тетрадь и заносить в нее формулировки законов и основных понятий, новые незнакомые термины и названия, формулы и уравнения реакций, математические зависимости и их выво-
ды и т. п. Во всех случаях, когда материал поддается си-
стематизации, составляйте графики, схемы, диаграм-
мы, таблицы. Они очень облегчают запоминание и уменьшают объем конспектируемого материала. Пока тот или иной раздел не усвоен, переходить к изучению новых разделов не следует. Краткий конспект курса будет полезен при повторении материала в период подготовки к экзамену. Изучение курса должно обязательно сопровождаться выполнением упражнений и решением задач (см. список рекомендованной литературы).
В пособии представлены специальные вопросы по топливу для инженеров и рассматриваются темы для технического профиля.
Однако при самостоятельной работе с учебным пособием рекомендуется обращаться к общедоступной справочной и учебной литературе для выяснения или уточнения новых терминов, понятий и определений. Большую пользу при изучении дисциплины может принести дополнительное чтение по списку рекомендуемой литературы.
3
1. ТЕРМОХИМИЧЕСКИЕ РАСЧЕТЫ
1.1. Тепловые эффекты реакций
Внутренняя энергия и энтальпия
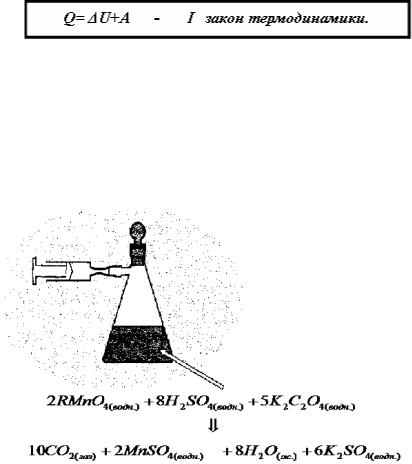
Фундаментальное значение в термодинамике имеют такие понятия, как система и внешняя среда. Система состоит из компонентов реакции, т. е. реагентов и продуктов реакции, а к внешней среде относится все остальное во вселенной, кроме системы. Системой может быть названо содержимое реакционного сосуда, ограниченное его стенками (рис. 1.1). Однако может не существовать определенной границы системы, как, например, в случае сублимации твердого СО2 (сухого льда), при которой он переходит в газообразный СО2; в этом случае может показаться, что система исчезает во внешней среде, однако молекулы СО2 по-прежнему составляют «систему».
Если система термически изолирована от внешней среды, изменения, происходящие в системе, называют адиабатическими, и обмен теплотой между системой и внешней средой отсутствует.
Многие реакции происходят при заданной, постоянной температуре и такие процессы называют изотермическими.
Для характеристики состояния системы и происходящих в ней изменений важно знать изменение таких функций состояния системы как внутренняя энергия (U), энтальпия (Н), энтропия (S) и изобарный потенциал (G).
Эти переменные называются функциями состояния, если известно, сколько вещества в системе, достаточно определить две функции состояния, чтобы стали известными все остальные функции состояния системы. Рассмотрим уравнение состояния идеального газа
P∙V=n R T, |
(1.1) |
4
где R (универсальная газовая постоянная) = 8,314 Дж/моль• К), V- объем, P - давление, T - температура, n - число молей.
Состояние системы характеризуется совокупностью параметров и свойств системы. Для системы характерны следующие параметры: давление (Р), температура (Т), объем (V), масса (m).
Имеются процессы, протекающие при постоянном значении некоторых параметров. При постоянной температуре (Т = const) – изотермические процессы, при постоянном давлении (Р = const) – изобарические, а при постоянном объеме (V = const) – изохорические процессы.
Абсолютные величины U, H, S, G не могут быть определены, однако можно измерить их изменение ΔU, ΔH, ΔS, ΔG в различных процессах. На основе этих параметров могут быть выведены другие переменные, позволяющие характеризовать состояние системы и происходящие в ней изменения.
Внутренняя энергия U – это суммарная энергия, которая характеризует общий запас энергии системы, включающий энергию колебаний атомов, их внутреннюю энергию, кинетическую и потенциальную энергию молекул, энергию движения электронов и т.д. Внутренняя энергия имеет размерность кДж/моль.
Внутренняя энергия системы (вещества или совокупности веществ) представляет собой ее полную энергию, которая складывается из энергии движения молекул, энергии движения ядер и электронов в молекулах и атомах, внутриядерной энергии, энергии межмолекулярного взаимодействия и т. п. (т. е. все виды энергии, кроме потенциальной и кинетической энергии системы как целого).
Предположим, что некоторая система за счет поглощения теплоты Q переходит из состояния 1 в состояние 2. В общем случае эта теплота расходуется на изменение внутренней энергии системы ΔU и на совершение работы против внешних сил
А:
5
Приведенное уравнение выражает закон сохранения энергии, т. е. означает, что сумма изменений внутренней
энергии и совершенной системой (или над нею) работы равна сообщенной ей (или выделенной ею) теплоте. Так, ес-
ли теплота сообщается газу в цилиндре, закрытом поршнем, то газ, во-первых, нагревается, т. е. его внутренняя энергия возрастает, а во-вторых, расширяется, т. е. производит работу подъема поршня А.
Рис. 1.1. Различие между системой и внешней средой на примере реакции, в ходе которой выделяется газ; газ собирается
вобъеме шприца, расширяющемся во внешнюю среду
входе реакции
Для химических реакций под работой против внешнихсил в основном подразумевается работа против внешнего давления. В первом приближении она равна произведению давления Р на изменение объема V системы:
6
А = P(V2 - V1) = PΔV. |
(1.2) |
При изохорном процессе, поскольку изменения объемасистемы не происходит, A=0. Тогда переходу системы из состояния 1 в состояние 2 отвечает равенство
Qv = U2 – U1 = ΔU.
Следовательно, если химическая реакция протекает при постоянном объеме, то выделение или поглощение теплоты Qv связано с изменением внутренней энергии системы.
Для химического процесса, протекающего изобарически, V представляет собой разность между суммой объемов продуктов реакции и суммой объемов исходных веществ. Так, для реакции, записываемой в общем виде
aA + bB+…=dD + eE+…, |
(1.3) |
изменение объема определяется равенством
ΔV=ΣVпрод - ΣVисх=(dVD + eVE +…) – (aVA - bVB +…),
где VA,VB…VD, VE - мольные объемы вещества А, В..., D, Е..., ΣVпрод – сумма мольных объемов продуктов реакции, ΣVисх – сумма мольных объемов исходных веществ.
Для изобарического процесса, следовательно, тепловой
эффект QP |
равен |
QP=ΔU + PΔV, |
|
|
|
|
QP=(U2 - U1) - P(V2 - V1) |
|
|
или |
|
QP=(U2 |
+ PV2) - (U1 + PV1). |
(1.4) |
Введем обозначение U + PV=H, |
|
|||
тогда |
Qp = H2 – H1 |
= ΔH. |
(1.5) |
|
1.2. Химическое сродство
Самопроизвольно могут протекать реакции, сопровождающиеся не только выделением, но и поглощением теплоты.
Реакция, идущая при данной температуре с выделением теплоты, при другой температуре идет в обратном направлении, т. е. с поглощением теплоты. Здесь проявляется диалек-
7
тический закон единства и борьбы противоположностей. С одной стороны, система стремится к упорядочению (агрегации), к уменьшению H, с другой стороны, система стремится к беспорядку (дезагрегации). Первая тенденция растет с понижением, а вторая — с повышением температуры. Тенденцию к беспорядку характеризует величина, которую называют энтропи-
ей.
Энтропия (S), так же как внутренняя энергия (U), энтальпия (H), объем V и др., является свойством вещества, пропорциональным его количеству. S, U, Н, V обладают аддитивными свойствами, т. е. при соприкосновении систем суммируются. Энтропия отражает движение частиц вещества и является ме-
рой неупорядоченности системы. Она возрастает с увеличе-
нием движения частиц: при нагревании, испарении, плавлении, расширении газа, при ослаблении или разрыве связей между атомами и т. п. Процессы, связанные с упорядоченностью системы: конденсация, кристаллизация, сжатие, упрочнение связей, полимеризация и т. п. - ведут к уменьшению - энтропии.
Таким образом, если при изохорическом процессе тепловой эффект реакции равен изменению внутренней энергии системы, то в случае изобарного процесса тепловой эффект равен изменению энтальпии системы. Для реакции, записываемой в общем виде (1.3), тепловой эффект
изохорного процесса- QV=ΔU=ΣUпрод–ΣUисх; изобарного процесса - QP=ΔH=ΣHпрод–ΣHисх.
Тепловой эффект реакции, протекающей при постоянном давлении, больше теплового эффекта реакции, протекающей при постоянном объеме, на величину работы расширения PΔV.
Поскольку подавляющее большинство химических реакций проходит при постоянном давлении, в дальнейшем основное внимание мы будем уделять изобарным процессам.
8
Энергетические эффекты. Тепловые эффекты реак-
цийопределяют как экспериментально, так и с помощью термохимических расчетов. Следует отметить, что мы не можем оценить абсолютных значений энтальпии и внутренней энергии. Однако для термохимических расчетов и экспериментального определения тепловых эффектов это несущественно, поскольку нас интересует изменение состояния системы, т. е. изменение значений Н и U.
Все процессы в электрохимии подразделяют на экзо-
термические и эндотермические. При экзотермических ре-
акциях теплота выделяется, т. е. уменьшается энтальпия, или внутренняя энергия системы, и значения ΔH и ΔU для них отрицательны. При эндотермических реакциях теплота поглощается, т. е. Н и U системы возрастают, а ΔH и ΔU имеют положительные значения.
Для того, чтобы можно было сравнивать тепловые эффекты различных процессов, термохимические расчеты обычно относят к одному молю соединения и условиям, принятым за стандартные. За стандартные принимают давление 1 атм. и температуру чаще всего 25 °С (298,15 °К). Стандартные тепловые эффекты принято обозначать ΔH°298.
Параметры, описывающие состояние системы, называются функциями состояния. Так, функциями состояния идеального газа, входящими в его уравнение состояния, являются давление, объем и температура. Энергия - также функция состояния. Важно помнить, что если заданы некоторые функции состояния, то остальные функции состояния могут принимать лишь вполне определенные значения. Например, задав давление и объем 1 моля идеального газа, мы тем самым вполне однозначно определим его температуру, а также энергию и другие функции состояния.
Одним из основных свойств любой функции состояния является независимость ее изменения от способа или пути изменения состояния системы. Например, если изменить объем-
9
