
Биологически активные вещества в биотехнологии
..pdfМинистерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Пермский национальный исследовательский политехнический университет»
Кафедра химии и биотехнологии
БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА В БИОТЕХНОЛОГИИ
Методические указания к лабораторным работам
Издательство Пермского национального исследовательского
политехнического университета
2016
1
Составители: Д.А. Казаков, Л.С. Пан, Л.В. Аникина, А.В. Портнова, Г.А. Козлова
УДК 577.19 (076.5) Б63
Рецензент канд. хим. наук, доцент М.М. Соколова
(Пермский национальный исследовательский политехнический университет)
Биологически активные вещества в биотехнологии : Б63 метод. указания к лабораторным работам / сост. Д.А. Казаков, Л.С. Пан, Л.В. Аникина, А.В. Портнова, Г.А. Козлова. – Пермь :
Изд-во Перм. нац. исслед. политехн. ун-та, 2016. 28 с.
Составлены в соответствии с федеральным государственным образовательным стандартом по направлению подготовки 19.03.01 «Биотехнология», рабочей программой дисциплины «Химия биологически активных веществ». Для каждой лабораторной работы дан перечень оборудования, реактивов, описаны методики проведения опытов и расчетов. Каждый раздел содержит вопросы для самостоятельной работы по теме.
Предназначены для студентов очной формы обучения по направлению 19.03.01 «Биотехнология».
© ПНИПУ, 2016
2
ОГЛАВЛЕНИЕ |
|
Введение................................................................................................. |
4 |
Техника безопасности при работе в биохимической |
|
лаборатории............................................................................................ |
4 |
Требования к оформлению отчетов по лабораторным |
|
работам................................................................................................... |
6 |
Раздел I. Углеводы, липиды, низкомолекулярные |
|
биорегуляторы..................................................................................... |
6 |
Лабораторная работа № 1. Количественное определение |
|
углеводов в растительной биомассе.................................................... |
6 |
Лабораторная работа № 2. Качественные реакции |
|
на антибиотики...................................................................................... |
9 |
Вопросы для самостоятельной работы |
|
к разделу «Углеводы, липиды, низкомолекулярные |
|
биорегуляторы» ................................................................................... |
11 |
Раздел II. Нуклеиновые кислоты................................................... |
12 |
Лабораторная работа № 3. Качественные реакции |
|
на компоненты нуклеиновых кислот................................................. |
12 |
Вопросы для самостоятельной работы к разделу |
|
«Нуклеиновые кислоты»..................................................................... |
15 |
Раздел III. Аминокислоты и белки................................................. |
16 |
Лабораторная работа № 4. Хроматографический метод |
|
определения аминокислот .................................................................. |
16 |
Лабораторная работа № 5. Качественные реакции |
|
на белки и аминокислоты ................................................................... |
19 |
Лабораторная работа№ 6. Количественноеопределение белка......... |
24 |
Вопросы для самостоятельной работы |
|
к разделу «Аминокислоты и белки» .................................................. |
26 |
Список литературы.............................................................................. |
27 |
|
3 |
ВВЕДЕНИЕ
В результате интенсивного развития химии биологически активных веществ в последние годы получены новые знания, сделавшие возможным практическое использование ранее неизвестных или малоизвестных соединений различных классов, нашедших применение в биотехнологии, медицине, косметике, сельском хозяйстве, пищевой промышленности и других отраслях. Промышленное освоение получения биологически активных соединений привело к разработке новейших технологий, объединенных общим названием «биотехнология».
Лабораторные работы проводятся с целью приобретения навыков и умений выделения биологических активных веществ из биологического материала, исследования их структуры и химических свойств с использованием необходимых реактивов и оборудования. Проведение лабораторных работ по химии биологически активных веществ позволяет закрепить теоретические знания о строении, пространственной структуре, биологических функциях и основах функционирования белков, нуклеиновых кислот, углеводов, липидов, низкомолекулярных биорегуляторов и продуктов жизнедеятельности клеток.
ТЕХНИКА БЕЗОПАСНОСТИ ПРИ РАБОТЕ
ВБИОХИМИЧЕСКОЙ ЛАБОРАТОРИИ
Влаборатории нужно соблюдать следующиеобщиетребования: 1. Работать только в спецодежде – халате и сменной обуви. 2. Приступать к работе только после вводного инструктажа и
первичного инструктажа на рабочем месте. Повторный инструктаж проводится не реже одного раза в шесть месяцев.
3.Перед работой внимательно ознакомиться с методикой проведения анализа и в соответствии с этим подготовить свое рабочее место.
4.Перед работой следует убедиться в том, что:
правильно уяснена методика;
4
правильно подготовлены приборы и оборудование;
взятые вещества соответствуют методике анализа;
всё расставлено так, чтобы было удобно достать, не вставая с места, и самое необходимое находится в пределах оптимальной рабочейзоны, соответствующейразмахусогнутойвлоктевомсуставеруки.
5.Работать только на своем месте.
6.Рабочее место содержать в чистоте, не загромождать его ненужными предметами.
7.Во время работы соблюдать тишину, порядок и чистоту.
8.Не допускать торопливости, невнимательности, беспорядочности и неряшливости.
9.Не покидать рабочее место во время проведения анализа, не оставлять без присмотра включенные приборы.
10.Запрещается выполнять работы, не связанные с непосредственной работой в лаборатории.
11.Соблюдать правила техники безопасности при работе с кислотами, щелочами, летучими и ядовитыми веществами, нагревательными приборами.
12.Соблюдать правила противопожарной безопасности.
13.Не наклоняться близко над открытыми склянками с реак-
тивами.
14.Работать с реактивами только над столом.
15.Пипетировать вещества только пипеткой с грушей или дозатором.
16.Запрещено выливать вещества в канализацию, для этого предусмотрены специальные банки.
17.Не пробовать на вкус в лаборатории любые вещества, даже если они кажутся вам знакомыми.
18.В лаборатории запрещается принимать пищу.
19.После работы обязательно вымыть руки с мылом.
20.После работы убрать все реактивы по местам, выключить все электроприборы, закрыть форточки, краны водоснабжения и протереть рабочий стол.
5
ТРЕБОВАНИЯ К ОФОРМЛЕНИЮ ОТЧЕТОВ ПО ЛАБОРАТОРНЫМ РАБОТАМ
Лабораторные работы оформляются каждым студентом в отдельной тетради согласно следующему плану:
1.Дата.
2.Название лабораторной работы.
3.Цель работы.
4.Принцип выделения, идентификации и количественного определения биомолекул, формулы и химизм реакций.
5.Методика выполнения работы.
6.Наблюдаемые явления и расчеты.
7.Выводы по работе с объяснением полученных результатов. В конце каждого раздела даются вопросы для самостоятельной
работы, которыепомогутприподготовкекзащителабораторныхработ.
РАЗДЕЛ I. УГЛЕВОДЫ, ЛИПИДЫ, НИЗКОМОЛЕКУЛЯРНЫЕ БИОРЕГУЛЯТОРЫ
Лабораторная работа № 1 КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ УГЛЕВОДОВ В РАСТИТЕЛЬНОЙ БИОМАССЕ
Цель работы: овладеть методами количественного определения содержания углеводов в растительном сырье.
В различных сортах яблок содержание углеводов может изменяться в диапазоне 6 148 мг/г с преобладанием отдельных моносахаридов, а также сахарозы.
Исследуемый материал: яблоки нескольких сортов.
Реактивы:
1.0,1 н раствор йода.
2.0,1 н раствор натрия гидроксида.
3.10%-ный раствор серной кислоты.
4.0,1 н раствор натрия тиосульфата.
5.1%-ный раствор крахмала.
6.10%-ный раствор соляной кислоты.
7.Сода.
6
Оборудование:
1.Плоскодонные колбы на 100 мл.
2.Водяная баня с термометром.
3.Воронки.
4.Фильтры бумажные.
5.Мерные колбы на 100 мл.
6.Пипетка на 5 мл.
7.Индикаторная бумага.
8.Мерные колбы на 50 мл.
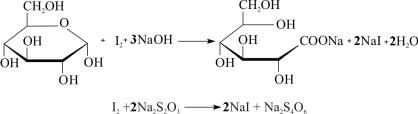
Ход работы: Берут навеску 5 г одного из сортов яблок, прибавляют 50 мл дистиллированной воды и экстрагируют на водяной бане при температуре 70 °С в течение 30 минут. Температуру бани не доводят до 100 °С, чтобы избежать гидролиза сахарозы, который может идти под влиянием имеющихся в яблоках кислот. По истечении времени нагревания вытяжку отфильтровывают через складчатый фильтр в мерную колбу на 100 мл. Остаток на фильтре несколько раз промывают горячей водой. Охлажденную до комнатной температуры вытяжку с промывными водами доводят водой до метки. Отбирают пипеткой 5 мл вытяжки и определяют в ней содержание глюкозы по Вильштеттеру. Метод определения основан на окислении альдегидной группы глюкозы йодом до карбоксильной группы в присутствии фруктозы и сахарозы, которые остаются неизменными.
Для определения глюкозы по Вильштеттеру к 5 мл исследуемого раствора прибавляют 7 мл 0,1 н раствора йода. Через 2 3 минуты при энергичном перемешивании медленно добавляют 10 мл 0,1 н раствора натрия гидроксида и оставляют стоять на 20 минут в темном месте. После этого раствор подкисляют 10%-ным раствором серной кислоты до кислой рН и остаток йода титруют 0,1 н раство-
7
ром натрия тиосульфата в присутствии индикатора – раствора крахмала. Титрование проводят как минимум в трех повторностях.
Далее 25 мл вытяжки из яблок помещают в коническую колбу, прибавляют 2 мл 10%-ной соляной кислоты и смесь выдерживают на кипящей водяной бане в течение 30 минут, затем раствор охлаждают, доводят до нейтральной рН с помощью соды, переливают в мерную колбу на 50 мл и доводят водой до метки. Далее снова определяют глюкозу по методу Вильштеттера. В этом случае будет определена суммарно свободная глюкоза и глюкоза, образовавшаяся при гидролизе сахарозы.
Указания к составлению отчета: Содержание свободной глюкозы в яблоке (мг/г) рассчитывают по результатам первого титрования (до гидролиза сахарозы) по формуле
Q1 = T·(V1 – V2)·k1/m,
где Т – титр 0,1 н раствора йода по глюкозе, равный 9 мг/мл; V1 – объем 0,1 н раствора йода, добавленный в аликвоту исследуемой вытяжки до гидролиза сахарозы, мл; V2 – объем 0,1 н раствора тиосульфата натрия, пошедший на титрование вытяжки до гидролиза сахарозы, мл; k1 – коэффициент пересчета, учитывающий соотношение объемов аликвоты вытяжки, взятой на анализ, и ее общего объема (k1 = 20); m – масса навески яблока, г.
Содержание сахарозы в яблоке (мг/г) рассчитывают совместно по результатам первого (до гидролиза сахарозы) и второго титрований (после гидролиза сахарозы) по формуле
Q2 = (T·(V3 – V4)·k2 – Q1)·Mс/(m·Мг),
где V3 – объем 0,1 н раствора йода, добавленный в аликвоту вытяжки, полученной после гидролиза сахарозы, мл; V4 – объем 0,1 н раствора тиосульфата натрия, пошедший на титрование вытяжки, полученной после гидролиза сахарозы, мл; k2 – коэффициент пересчета, учитывающий соотношение объемов аликвоты вытяжки, взятой на анализ, ее общего объема и разведение, произведенное на стадии гидролиза сахарозы; Mс, Мг – соответственно молярные массы сахарозы и глюкозы, г/моль.
Напишите уравнение реакции гидролиза сахарозы.
8

Лабораторная работа № 2 КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АНТИБИОТИКИ
Цель работы: формирование навыков анализа различных групп антибиотиков.
Исследуемый материал: порошки эритромицина, тетрациклина и левомицетина.
Реактивы:
1.Концентрированная серная кислота.
2.5%-ный раствор FeCl3.
3.10%-ный раствор NaOH.
Оборудование:
1.Штатив с пробирками.
2.Пипетки.
Ход работы:
1.Качественная реакция на эритромицин. Эритромицин
относится к группе антибиотиков-макролидов, содержащих в молекуле макроциклическое лактонное кольцо. Продуцируется акти-
номицетами Streptomyces erythreus.
CH3 |
|
|
CH3 |
|
O |
O |
OH |
|
OH |
CH3 |
O |
N |
OHO |
O |
CH3 |
H3C CH3 |
|
|
|
 OHOHO
OHOHO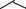
 O O
O O

эритромицин
Метод основан на образовании окрашенных продуктов окисления под действием концентрированных кислот.
9
К 0,02 г эритромицина добавить 2 мл концентрированной серной кислоты, появляется красно-коричневое окрашивание.
2. Качественные реакции на тетрациклин. Тетрациклины – группа антибиотиков, имеющая конденсированную четырехциклическую систему под общим названием тетрациклин. Тетрациклины были выделены из актиномицетов Streptomyces aureoaciens и Streptomyces rimosus. В основе действия тетрациклинов лежит подавление ими биосинтеза белка микробной клетки на уровне рибосом.
CH3 |
H3C |
N |
CH3 |
|
|
||
|
|
|
OH |
OH |
|
|
|
|
OHOHO |
C NH2 |
|
OH O |
O |
||
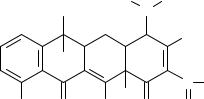
тетрациклин
Метод основан на свойстве концентрированной серной кислоты образовывать ангидропроизводные тетрациклинов. При последующем добавлении хлорида железа проявляется окраска, обусловленная наличием фенольных гидроксилов в молекуле тетрациклина.
0,1 г тетрациклина поместить в пробирку, прибавить 2 мл концентрированной серной кислоты. При добавлении 1 мл воды окраска становится фиолетовой в случае тетрациклина, красной в случае окситетрациклина и зеленой в случае хлортетрациклина. При добавлении 1 2 капель раствора хлорида железа окраска переходит в коричневую или красно-коричневую.
3. Качественная реакция на левомицетин. Левомицетин – синтетическое вещество, идентичное природному антибиотику хлорамфениколу, являющемуся продуктом жизнедеятельности актиномицетов Streptomyces venezuelae. Механизм антимикробного действия связан с нарушением синтеза белков микроорганизмов.
10
